- Trang chủ
- Sách y học
- Bài giảng sinh lý bệnh
- Các nguyên nhân rối loạn cân bằng acid base trên lâm sàng
Các nguyên nhân rối loạn cân bằng acid base trên lâm sàng
Cách điều trị tốt nhất cho nhiễm acid hoặc nhiễm kiềm là điều chỉnh lại tình trạng gây ra sự bất thường. Điều này thường rất khó, đặc biệt đối với các bệnh mạn tính làm suy yếu chức năng của phổi hoặc gây ra suy thận.
Biên tập viên: Trần Tiến Phong
Đánh giá: Trần Trà My, Trần Phương Phương
Bất kỳ nguyên nhân nào làm giảm thông khí ở phổi đều làm tăng pCO2 dịch ngoại bào. Điều này làm tăng nồng độ H2CO3 và H+ dẫn đến nhiễm toan. Bởi vì nguyên nhân nhiễm toan là bất thường của hô hấp nên trường hợp này được gọi là nhiễm toan hô hấp.
Toan hô hấp
Toan hô hấp xảy ra trong các bệnh lý có tổn thương trung tâm hô hấp hoặc các bệnh lý giảm khả năng đào thải CO2 của phổi. Ví dụ: tổn thương trung tâm hô hấp ở hành não có thể dẫn đến nhiễm toan hô hấp. Ngoài ra, tắc nghẽn đường hô hấp, viêm phổi, khí thũng, giảm diện tích màng trao đổi khí của phổi, các yếu tố cản trở trao đổi khí giữa máu và không khí phế nang đều gây nhiễm toan hô hấp.
Trong nhiễm toan hô hấp, các đáp ứng bù trừ gồm có (1) hệ đệm của dịch cơ thể và (2) thận, đòi hỏi vài ngày để bù trừ cho rối loạn.
Tăng thông khí và giảm pCO2 dẫn đến nhiễm kiềm hô hấp
Nhiễm kiềm hô hấp là do thông khí quá mức của phổi. Hiếm khi điều này xảy ra do các tình trạng bệnh lý. Tuy nhiên bệnh tâm thần-tâm lý có thể làm tăng hô hấp đến mức dẫn đến tình trạng nhiễm kiềm.
Một type sinh lý của nhiễm kiềm hô hấp xảy ra khi một người lên độ cao lớn. Nồng độ O2 thấp kích thích hô hấp, gây mất CO2 dẫn đến kiềm hô hấp nhẹ. Giống như trên,cơ thể đáp ứng bù trừ nhờ hệ đệm dịch cơ thể và thận tăng bài tiết HCO3- .
Nhiễm toan chuyển hóa là do giảm nồng độ HCO3- dịch ngoại bào
Thuật ngữ nhiễm toan chuyển hóa được dùng cho tất cả các dạng nhiễm toan bên cạnh nguyên nhân do tăng CO2 trong dịch cơ thể. Toan chuyển hóa là kết quả của một số nguyên nhân tổng quát sau: thận giảm chức năng bài tiết acid hình thành trong cơ thể, cơ thể tạo ra quá nhiều acid trong trao đổi chất, uống hoặc tiêm truyền các chất có tính acid cho cơ thể, mất baso trong các dịch cơ thể, điều này có tác dụng giống như thêm acid cho cơ thể. Một số tình trạng cụ thể gây toan chuyển hóa sẽ được mô tả ở phần sau.
Nhiễm toan ống thận. Nhiễm toan ống thận là do khiếm khuyết trong bài tiết H+ hoặc tái hấp thu HCO3- hoặc cả hai. Những rối loạn này nhìn chung chia làm 2 type: (1) suy giảm tái hấp thu HCO3- ở ống thận làm mất HCO3- vào nước tiểu, (2) mất khả năng bài tiết H+ của ống thận, đây là cơ chế làm cho bình thường nước tiểu có tính acid, sự mất khả năng này làm kiềm nước tiểu. Hai rối loạn trên gây ra không đủ trung hòa acid cơ thể và giảm bài tiết NH4+, do đó gây ra tích lũy acid trong các dịch cơ thể. Một số nguyên nhân gây nhiễm toan ống thận gồm có suy thận mãn tính, bài tiết thiếu aldosterone (bệnh Addison), một số rối loạn di truyền dẫn đến suy giảm chức năng ống thận, chẳng hạn như hội chứng Fanconi.
Tiêu chảy. Tiêu chảy là một trong những nguyên nhân thường xuyên nhất gây nhiễm toan chuyển hóa, nhiễm toan là do mất một lượng lớn Natribicarbonat vào phân. Dịch tiết đường tiêu hóa chứa nhiều bicarbonat, kết quả là tiêu chảy gây mất HCO3- của dịch cơ thể. ảnh hưởng này cũng tương tự như mất HCO3- vào nước tiểu. Đây là tình trạng toan chuyển hóa nghiêm trọng có thể dẫn đến tử vong, đặc biệt là trẻ em.
Nôn (các chất trong ruột). Nôn các chất trong dạ dày gây mất acid và có xu hướng gây nhiễm kiềm vì dịch tiết dạ dày có tính acid cao. Tuy nhiên, đôi khi xảy ra nôn một lượng lớn các chất trong ruột gây mất một lượng lớn bicarbonat gây ra nhiễm toan chuyển hóa giống như tiêu chảy.
Đái tháo đường. Đái tháo đường xảy ra do sự giảm bài tiết insulin của tuyến tụy (type 1) hoặc lượng insulin không đủ để bù đắp cho sự giảm nhạy cảm tác dụng của insulin (type 2). Trong trường hợp không đủ insulin dẫn đến cản trở sử dụng glucose trong trao đổi chất. Thay vào đó, các chất béo được cắt thành acid acetoacetic, các axit này được chuyển hóa bởi các mô sinh năng lượng. Với bệnh tiểu đường nặng, nồng độ acid acetoacetic máu tăng lên rất cao gây toan chuyển hóa nặng. Để bù trừ cho toan chuyển hóa nặng này, một lượng lớn acid được bài tiết vào nước tiểu, có thể lên tới 500mmol/ngày.
Uống acid. Hiếm khi có một lượng lớn acid trong thực phẩm bình thường. Tuy nhiên, đôi khi nhiễm toan chuyển hóa nặng là do uống một lượng lớn chất độc có tính acid.
Các chất này bao gồm acetylsalicylics (aspirin) và methyl alcohol (dạng chuyển hóa là acid formic).
Suy thận mạn tính. Khi chức năng thận suy giảm rõ rệt gây ra tích lũy anion của các acid yếu trong dịch cơ thể do không được đào thải qua thận. Ngoài ra, mức lọc cầu thận giảm gây ra giảm bài tiết phosphat và NH4+, giảm tái hấp thu HCO3- vào dịch cơ thể. Do đó suy thận mạn tính có thể gây ra toan chuyển hóa nặng.
Nhiễm kiềm chuyển hóa là do tăng nồng độ HCO3- dịch ngoại bào
Giữ quá mức HCO3- hoặc mất H+ trong cơ thể gây ra nhiễm kiềm chuyển hóa. Nhiễm kiềm chuyển hóa không phổ biến như toan chuyển hóa, nhưng phần sau đây sẽ mô tả một số nguyên nhân gây kiềm chuyển hóa.
Sử dụng thuốc lợi tiểu (trừ thuốc ức chế Carbonic Anhydrase). Các thuốc lợi tiểu đều gây tăng lưu lượng dịch lọc dọc theo ống thận, điều đó làm tăng lưu lượng ở ống lượn xa và ống góp. Hiệu ứng này dẫn đến tăng tái hấp thu Na+ từ các phần của nephron. Vì sự tái hấp thu Na+ kèm theo bài tiết H+ nên sự tăng cường tái hấp thu Na+ dẫn đến tăng bài tiết H+ và tăng tái hấp thu bicarbonat. Những thay đổi này dẫn tới nhiễm kiềm, đặc trưng bởi tăng nồng độ HCO3- dịch ngoại bào.
Thừa aldosterone. Khi một lượng lớn Aldosterone được bài tiết bởi tuyến thượng thận sẽ gây ra nhiễm kiềm chuyển hóa nhẹ. Giống như bàn luận ở phần trên, aldosterone làm tăng tái hấp thu Na+ ở ống lượn xa và ống góp, đồng thời kích thích bài tiết H+ ở tế bào xen ống góp. Điều này làm tăng bài tiết H+ qua thận dẫn tới nhiễm kiềm.
Nôn (các chất ở dạ dày). Nôn các chất chỉ ở dạ dày, không liên quan tới các chất ở đường tiêu hóa dưới dạ dày, gây mất HCl do các tế bào niêm mạc dạ dày bài tiết. Kết quả là mất acid dịch ngoại bào dẫn tới nhiễm kiềm chuyển hóa. Nhiễm kiềm này thường xảy ra đặc biệt là ở trẻ sơ sinh có hẹp môn vị do phì đại cơ thắt.
Uống thuốc có tính kiềm. Một nguyên nhân phổ biến gây ra nhiễm kiềm chuyển hóa là uống thuốc có tính kiềm như natribicarbonate, để điều trị viêm dạ dày hoặc loét dạ dày tá tràng.
Điều trị rối loạn cân bằng acid - base
Cách điều trị tốt nhất cho nhiễm axit hoặc nhiễm kiềm là điều chỉnh lại tình trạng gây ra sự bất thường. Điều này thường rất khó, đặc biệt đối với các bệnh mạn tính làm suy yếu chức năng của phổi hoặc gây ra suy thận. Trong những trường hợp này, có nhiều chất khác nhau có thể được sử dụng để trung hòa lượng axit quá ngưỡng hoặc căn cứ vào chất lưu ngoại bào.
Để trung hòa lượng axit vượt ngưỡng, lượng lớn natri cacbonnat có thể được đưa vào bằng đường uống. Muối natri cacbonat được hấp thụ ở đường ruột vào máu và tăng lượng HCO3- của hệ thống đệm bicarbonate, vì thế làm tăng pH gần đến bình thường. Natri cacbonat có thể được truyền tĩnh mạch nhưng vì có những tác động nguy hiểm tiềm ẩn của cách điều trị này, do đó mà các chất khác thường xuyên được sử dụng thay thế như natri lactat và natri gluconate. Lượng chất lactate và gluconate có trong cơ bắp được chuyển hóa trong cơ thể, để lại natri trong dịch ngoại bào dưới natri bicacbonat và vì thế làm tăng lên pH của dịch ngoại bào gần đến bình thường.
Đối với việc điều trị của chứng nhiễm kiềm, amoni clorua có thể được cung cấp bằng đường uống. Khi chất này được hấp thụ vào máu, lượng amoni được chuyển hóa ở gan thành urê. Phản ứng này giải phóng HCl,là chất sẽ ngay lập tức phản ứng hệ đệm của cơ thể để chuyển sự tập chung của H+ thành đặc tính của axit. Amoni clorua cũng có thể được truyền tĩnh mạch nhưng NH4+ rất độc hại và quá trình này có thể trở nên vô cùng nguy hiểm. Phương pháp trị liệu phù hợp nhất là đảo nghịch lại nguyên nhân cơ bản gây ra chứng nhiễm kiềm. Ví dụ nếu nhiễm kiềm chuyển hóa liên qun đến việc giảm thể tích dịch ngoại bào, nhưng tim không bị ảnh hưởng thì giải pháp truyền một lượng đầy đủ phù hợp huyết thanh nhân tạo thường có hiệu quả trong việc trị liệu chứng nhiễm kiềm.
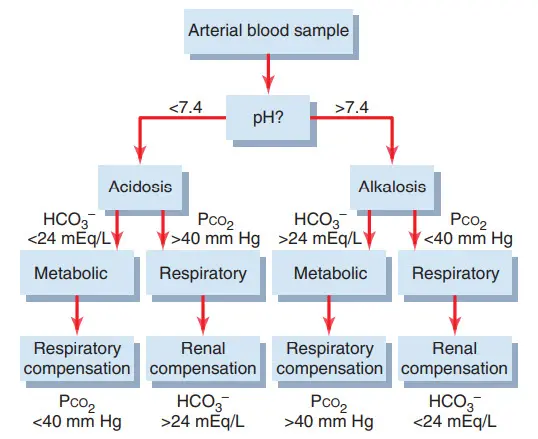
Bảng. Phân tích rối loạn acid - base. Nếu sự đền bù khác rõ rệt từ những hiện thị ở dưới hình thì ta nên nghi ngờ một nhiễm toan kiềm hỗn hợp
Các phép đo lâm sàng và phân tích các rối loạn axit-base
Giả thiết phù hợp của rối loạn axit đòi hỏi phải có sự chẩn đoán chính xác. Rối loạn axit đơn giản được miêu tả trước đó có thể được chẩn đoán bằng việc phân tích ba phương pháp từ một mẫu máu: pH, HCO3- huyết thanh, và PCO2.
Sự chẩn đoán này liên quan đến rất nhiều bước, được nói rõ ở bảng. Bằng việc kiểm tra độ pH, có thể biết được bệnh nhân bị rối loạn axit hay rối loạn kiềm. pH nhỏ hơn 7.4 cho thấy bệnh nhân nhiễm axit, trong khi pH lớn hơn 7.4 chỉ ra bệnh nhân nhiễm kiềm.
Bước thứ hai là phân tích PCO2 huyết tương và nồng độ HCO3-. Giá trị bình thường của PCO2 vào khoảng 40 mm Hg và của HCO3- là 24mEq/L. Nếu rối loạn được mô tả như là nhiễm toan và PCO2 huyết tương tăng lên thì phải có một thành phần đường hô hấp nhiễm toan. Sau khi bù bởi thận, nồng độ HCO3- huyết thanh ở đường hô hấp nhiễm toan sẽ có xu hướng tăng lên trên mức bình thường. Vì thế giá trị kì vọng cho một nhiễm toan hô hấp đơn giản sẽ giảm pH, tăng PCO2 và tăng nồng độ HCO3- huyết thanh sau mỗi lần bù bởi thận từng phần .
Đối với nhiễm toan chuyển hóa, sẽ có sự giảm PH huyết thanh. Tuy nhiên với nhiễm toan chuyển hóa thì sự bất bình thường đầu tiên là việc giảm nồng độ HCO3- huyết thanh. Vì thế nếu pH thấp tương tác với nồng độ HCO3- thấp thì phài có một thành phần chuyển hóa axit. Trong nhiễm toan chuyển hóa đơn thuần, lượng PCO2 giảm đi vì một phần bù đắp vào hô hấp, trái ngược với việc nhiễm toan hô hấp mà trong đó lượng PCO2 tăng lên. Vì thế, đối với việc toan chuyển hóa đơn giản, chúng ta thường mong tìm thấy hàm lượng độ pH thấp, nồng độ HCO3- thấp và sự giảm đi PCO2 sau mỗi lần bù đắp bởi hô hấp.
Quá trình phân ra các loại nhiễm kiềm liên quan đến các bước cơ bản. Đầu tiên, nhiễm kiềm chỉ rằng có sự tăng lên của pH huyết thanh. Nếu sự tăng lên này tương tác với việc giảm PCO2 thì phải có một thành phần đường hô hấp nhiễm kiềm. Nếu sự tăng lên pH tương tác với sự tăng lên của HCO3- thì phải có một thành phần chuyển hóa sang kiềm. Vì thế trong nhiễm kiềm hô hấp đơn giản, chúng ta mong muốn tìm thấy sự tăng lên của pH, sự giảm đi của PCO2 và việc giảm nồng độ HCO3- trong huyết thanh. Trong nhiễm kiềm chuyển hóa, ta mong muốn thấy sự tăng lên pH, HCO3- và sự tăng lên của PCO2.
Rối loạn cân bằng acid-base và việc sử dụng đồ thị trong chẩn đoán
Trong một vài trường hợp, rối loạn axit base không kèm theo phản ứng bù lại phù hợp. Khi tình huống này xảy ra, sự bất thường được phản ánh như một sự rối loạn hỗn hợp toan kiềm, điều này có nghĩa là sẽ có hai hoặc nhiều hơn những nguyên nhân căn bản gây ra sự rối loạn toan kiềm. Ví dụ, một bệnh nhân có độ pH thấp sẽ được phân loại acidotic .Nếu rối loạn là chuyển hóa trung gian, việc này cũng đi kèm với nồng độ HCO3 huyết tương thấp và sau khi có sự bù đắp bởi hô hấp thích hợp một lượng thấp PCO2. Tuy nhiên nếu độ pH thấp và nồng độ HCO3 huyết tương thấp liên quan với lượng PCO2 tăng lên thì tình trạng bệnh sẽ được cho là có một thành phần hô hấp bị nhiễm toan cũng như là một thành phần chuyển hóa. Vì thế chứng rối loạn này sẽ được phân loại là nhiễm toan hỗn hợp. Rối loạn này có thể xảy ra, ví dụ nếu một bệnh nhân bị thiếu hụt HCO3 cấp tính ở đường ruột do bệnh tiêu chảy gây ra (toan chuyển hóa) và khí thũng (toan hô hấp).
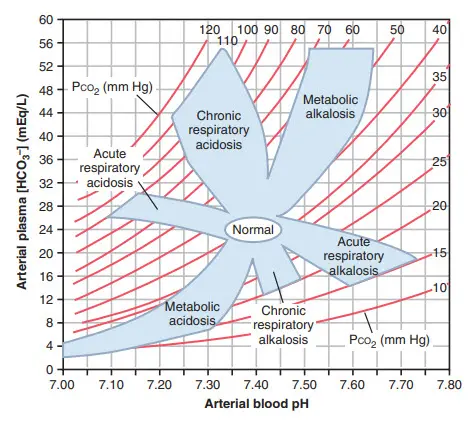
Hình. Biểu đồ axit-base cho thấy giá trị pH máu động mạch, HCO3- và PCO2 huyết tương động mạch. Vòng tròn mở trung tâm cho thấy giới hạn gần đúng đối với tình trạng axit base ở người bình thường. Các khu vực bóng mờ trong hình chụp ảnh cho thấy giới hạn gần đúng đối với sự bù đắp bình thường do các rối loạn chuyển hóa và hô hấp đơn giản gây ra. Đối với các giá trị nằm ngoài vùng bóng mờ, người ta nên nghi ngờ có rối loạn hỗn hợp axit-bazơ.
Một cách tiện lợi để chẩn đoán rối loạn axit base là sử dụng đồ thị axit base, như trên hình. biểu đồ này có thể được sử dụng để xác định là nhiễm toan hay nhiễm kiềm, cũng như xác định mức độ nghiêm trọng của nó. Trong biểu đồ axit base này thì pH, nồng độ HCO3 và các giá trị PCO2 cắt nhau theo công thức Henderson - Hasselbalch. vòng tròn mở trung tâm cho thấy giá trị bình thường và sự sai lệch có thể vẫn được cân nhắc trong dãy thông thường. phần diện tích đổ bóng của biểu đồ cho thấy 95% giới hạn chắc chắn cho sự bù đắp thông thường đối với sự chuyển hòa bình thường và sự rối loạn hô hấp. Khi sử dụng đồ thị này, có thể cho rằng thời gian đủ trôi qua cho một phản ứng bù đắp là: bù đắp thông khí cho sự rối loạn chuyển hóa ban đầu là từ 6 đến 12 giờ và sự bù đắp chuyển hóa cho rối loạn hô hấp đầu tiên là 3 đến 5 ngày. nếu giá trị nằm trong vùng đổ bóng có nghĩa là có một sự rối loạn axit base đã diễn ra. ngược lại, nếu các giá trị của độ pH, bicarbonate hoặc PCO2 nằm ngoài vùng đổ bóng có nghĩa là bệnh nhân có thể đã nhiễm toan kiềm hỗn hợp.
Việc nhận ra một giá trị axit base nằm trong vùng đổ bóng không luôn luôn có nghĩa là một rối loạn axit diễn ra là rất quan trọng. Khi nhớ rõ lưu ý này thì biểu đồ axit cơ bản có thể được sử dụng như là công cụ nhanh chóng cho việc xác định các dạng cụ thể và mức độ nghiêm trọng của rối loạn acd-base.
Ví dụ, giả thiết rằng huyết thanh chính từ một bệnh nhân có các giá trị như sau: pH 7.30, sự tập trung huyết thanh HCO3 là 12 mEq/L và huyết thanh PCO2 là 25 mm Hg. với các giá trị này, chúng ta có thể nhìn vào biểu đồ và thấy rằng bệnh nhân nhiễm axit chuyển hóa đơn giản, với sự bù đắp hô hấp phù hợp để làm giảm lượng PCO2 từ giá trị bình thường 40 mm Hg xuống còn 25 mm Hg.
Một ví dụ thứ hai là một bệnh nhân với các chỉ số như sau: độ pH là 7.15, nồng độ HCO3 là 7 mEq/L, và PCO2 là 50 mm Hg. Trong ví dụ này, bệnh nhân bị nhiễm acidotic và có sự xuất hiện của một thành phẩn chuyển hóa vì nồng độ HCO3 thấp hơn giá trị thông thường là 24 mEq/L. tuy nhiên sự bù trừ bởi hô hấp mà thông thường làm giảm lượng PCO2 sẽ không còn nữa và lượng PCO2 sẽ tăng nhẹ, cao hơn gía trị bình thường ( giá trị bình thường là 40 mm Hg). Phát hiện này phù hợp với sự rối loạn axit base hỗn hợp bao gồm toan chuyển hóa cũng toan hô hấp.
Đồ thị axit base là một cách nhanh chóng để tiếp cận phân loại và đánh giá mức độ của rối loạn, một bệnh gây ra sự bất bình thường của pH, PCO2 và nồng độ bicarbonate. Trong các tài liệu ghi chép lâm sàng thì tiền sử bệnh nhân và các phát hiện vật lí khác cũng cung cấp những manh mối quan trọng liên quan gây ra và cách điều trị chứng rối loạn axit base.
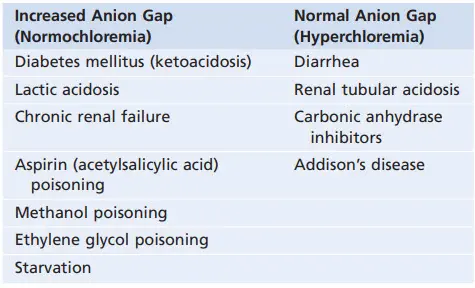
Bảng. Toan chuyển hóa liên quan tới khoảng trống anion
Sử dụng khoảng trống anion để chấn đoán rối loạn acid-base
Nồng độ các anion và cation trong huyết tương phải cân bằng để trung hòa về điện. Do đó, không có thực “ khoảng trống anion” trong huyết tương. Tuy nhiên chỉ có một số các cation và anion thường xuyên được đo trong lâm sàng và trong phòng thí nghiệm. Các cation thường được đo là Na + và anion thường được đo là Cl- và HCO3-. “ khoảng trống anion” (chỉ là khái niệm chẩn đoán) là sự khác biệt giữa cation phụ và nồng độ phụ , được tính như sau:
Khoảng trống anion huyết thanh = Na+ - Cl- -HCO3- = 144 - 24 - 108 = 12 mEq/L
Khoảng trống anion tăng khi mà các anion phụ tăng hoặc các cation phụ giảm. Các cation không đo quan trọng nhất gồm canxi, magie và kali, các anion không đo quan trọng chủ yếu là albumin, photphat, sulphat và các anion hữu cơ khác. Thông thường anion phụ vượt quá các cation phụ và khoảng trống anion nằm trong khoảng từ 8 đến 16 mEq/l.
Khoảng trống anion được sử dụng chủ yếu trong việc chẩn đoán các nguyên nhân khác nhau của nhiễm toan chuyển hóa. Trong nhiễm toan chuyển hóa, nồng độ HCO3- huyết tương giảm. Nếu nồng độ Na huyết tương không đổi , nồng độ anion (Cl- hoặc anion phụ khác) phải tăng để duy trì cân bằng điện tích. Nếu Cl- huyết tương tăng tỉ lệ thuận với sự giảm HCO3- huyết tương thì khoảng trống anion không thay đổi. Điều này thường được gọi là hyperchloreimic toan chuyển hóa.
Nếu HCO3- huyết tương giảm không kèm theo tăng Cl- thì phải có tăng nồng độ của các anion phụ và do đó khoảng trống anion tăng. Toan chuyển hóa do dư thừa acid (ngoài HCl) chẳng hạn như acid lactic hoặc ketoacid kết hợp với một khoảng trống anion huyết tương tăng do giảm HCO3- không tương xứng với mức độ tăng của Cl-. Một số ví dụ về toan chuyển hóa có khoảng trống anion bình thường hoặc tăng được trình bày ở bảng.
Bằng cách tính toán khoảng trống anion mà chúng ta có thể thu hẹp được một số nguyên nhân gây toan chuyển hóa.
Bài viết cùng chuyên mục
Sinh lý bệnh hội chứng thượng thận sinh dục
Trong hội chứng sinh dục thượng thận, sự bài tiết 17 ketosteroids trong nước tiểu có thể lên tới 10 đến 15 lần so với bình thường, nó có thể được sử dụng trong chẩn đoán bệnh.
Cường aldosterol nguyên phát và hội chứng Conn’s
Cường aldosterol nguyên phát là thỉnh thoảng có đợt liệt cơ do hạ kali huyết, tình trạng tê liệt là do tác dụng của thuốc làm nồng độ kali ngoại bào thấp trên hoạt động dẫn truyền sợi thần kinh.
Tăng chức năng tuyến thượng thận tác dụng lên chuyển hóa cacbohydrat và protein
Tác dụng của glucocorticoid trên dị hóa protein thường rõ trong hội chứng Cushing, làm giảm rất nhiều protein mô gần như ở khắp mọi nơi trong cơ thể với ngoại trừ của gan.
Tăng chức năng tuyến thượng thận và hội chứng Cushing
Tiết ACTH quá mức là nguyên nhân thường gặp nhất của hội chứng Cushing và được đặc trưng bởi nồng độ cao ACTH và cortisol trong huyết tương.
Sinh lý bệnh của suy thượng thận và bệnh lý Addison
Lượng lớn của glucocorticoid đôi khi tiết ra để đáp ứng với các loại stress về thể chất hoặc tinh thần, bệnh Addison, đầu ra của glucocorticoid không tăng trong khi bị stress.
Sinh lý bệnh của bệnh đần độn
Thiếu hụt bẩm sinh tuyến giáp, tuyến giáp không có khả năng sản xuất hormon giáp do khiếm khuyết một gen của tuyến, hoặc do thiếu hụt iod trong chế độ ăn.
Sinh lý bệnh của suy giáp
Suy giáp thường có căn nguyên là tự miễn, có các kháng thể chống lại tuyến giáp, nhưng trong trường hợp này kháng thể kháng giáp phá hủy tuyến giáp hơn là kích thích tuyến giáp.
Sinh lý bệnh của cường giáp
Trạng thái dễ bị kích động, nhiệt độ, tăng tiết mồ hôi, sút cân nhẹ đến nhiều, mức độ tiêu chảy khác nhau, yếu cơ, hốt hoảng,bồn chồn hoặc các rối loạn tâm thần khác, mệt mỏi vô cùng nhưng khó ngủ và run tay.
Giảm bài tiết hormone GH gây ra các biến đổi liên quan đến sự lão hóa
Kiểu hình theo độ tuổi chủ yếu là kết quả của việc giảm lắng đọng protein ở các mô cơ thể và thay vào đó là tăng lắng đọng mỡ ở các mô này, các ảnh hưởng thực thể và sinh lý làm tăng nếp nhăn, giảm chức năng một số cơ quan.
Bất thường bài tiết hormone tăng trưởng (GH)
Bất thường bài tiết hormone tăng trưởng gây ra suy tuyến yên trước, chứng lùn, bệnh khổng lồ, bệnh to cực chi, suy tuyến yên trước ở người trưởng thành.
Định lượng nồng độ hormone trong máu
Phương pháp rất nhạy đã định lượng các hormone, tiền thân của chúng và sản phẩm chuyển hóa của chúng, bổ sung thêm nhiều phương pháp, như xét nghiệm miễn dịch gắn enzyme.
Diễn biến khi cơ thể tiếp xúc với quá lạnh
Trừ khi được điều trị ngay lập tức, một người ngâm trong nước lạnh thường chết sau 20 đến 30 phút, do ngừng tim hoặc rung tim. Lúc đó thân nhiệt sẽ giảm xuống mức 77 độ F.
Sinh lý bệnh của say nóng
Trong số những thay đổi sinh lý quan trọng trong qua trình thích nghi với tăng nhiệt độ gồm tăng lượng mồ hôi tối đa gấp 2 lần, tăng thể tích huyết tương, và giảm lượng muối mất qua mồ hôi và nước tiểu.
Các đặc trưng trong trạng thái sốt
Khi điểm nhiệt chuẩn của trung tâm điều nhiệt đột ngột thay đổi từ mức bình thường lên mức cao hơn, thân nhiệt sẽ phải mất nhiều giờ để đạt được điểm nhiệt chuẩn mới.
Bất thường trong điều hòa thân nhiệt cơ thể người
Một số chất gây sốt, khi được tiêm vào vùng dưới đồi, có thể ngay lập tức và trực tiếp tác động trên đây làm tăng điểm nhiệt chuẩn, các chất gây sốt khác tác động gián tiếp và có thể mất vài giờ để chúng gây tác dụng.
Nhu cầu Vitamins của cơ thể
Vitamin là một hợp chất hữu cơ với số lượng nhỏ cần thiết cho chuyển hóa bình thường mà cơ thể không tự tổng hợp được, sự thiếu hụt vitamin trong khẩu phần có thể gây ra những rối loạn chuyển hóa nghiêm trọng.
Cơ chế bệnh sinh của gầy mòn chán ăn và suy nhược
Kho dự trữ chất béo hoàn toàn cạn kiệt, và chỉ còn nguồn năng lượng duy nhất là protein, thời điểm này, kho protein dự trữ một lần nữa bước vào giai đoạn suy giảm nhanh chóng.
Hiểu biết toàn diện cơ chế bệnh sinh của béo phì
Nguy cơ béo phì ảnh hưởng đến nhiều bệnh lý khác nhau như xơ gan, tăng huyết áp, bệnh lý tim mạch, đột quỵ, và bệnh thận xuất hiện liên quan nhiều tới béo tạng (béo bụng) hơn là tăng dự trữ mỡ dưới da, hoặc dự trữ chất béo phần thấp cơ thể như là hông.
Phòng chống xơ vữa động mạch
Giảm 1 mg/dl LDL cholesterol trong huyết tương, thì tương đương giảm 2% tỷ lệ tử vong do bệnh tim xơ vữa động mạch. Do đó, các biện pháp phòng ngừa thích hợp có giá trị hiệu quả trong làm giảm các cơn đau tim.
Những yếu tố chính gây xơ vữa động mạch
Gây xơ vữa động mạch bằng cách làm tăng nồng độ LDLs trong huyết tương, yêu tố khác như là tăng huyết áp, dẫn tới xơ vữa động mạch do làm tổn thương lớp nội mạc mạch máu và những thay đổi khác lên các mô mạch máu.
Vai trò của Cholesterol và Lipoprotein trong xơ vữa động mạch
Yếu tố quan trọng gây xơ vữa động mạch là nồng độ LDLs cholesterol trong máu cao, LDLs cholesterol trong huyết tương cao, tăng lên do nhiều yếu tố, đặc biệt là do ăn nhiều chất béo bão hòa.
Cơ chế bệnh sinh của xơ vữa động mạch
Các mảng xơ vữa bám vào còn ảnh hưởng tới dòng máu chảy, bề mặt thô ráp của chúng làm cho các cục máu đông phát triển tại đó, tạo thành huyết khối tại chỗ hoặc cục máu đông.
Béo phì: sự lắng đọng chất béo dư thừa
Di truyền ảnh hưởng tới trung tâm não điều hòa năng lượng hay những con đường mà kiểm soát năng lượng sử dụng hoặc năng lượng được dự trữ có thể là nguyên nhân gây ra béo phì di truyền ở người.
Cơ chế bệnh sinh của rối loạn tiêu hóa
Cơ chế bệnh sinh của rối loạn tiêu hóa, nôn mửa và buồn nôn, tắc nghẽn đường tiêu hóa, đầy hơi ứ khí đường tiêu hóa.
Cơ chế bệnh sinh của rối loạn đại tràng
Bệnh rối loạn đại tràng bao gồm táo bón, bệnh tiêu chảy do tâm lý, bệnh tiêu chảy do viêm đại tràng và liệt đại tiện ở những người bị chấn thương tủy sống.
Kém hấp thu bởi niêm mạc ruột non - Sprue
Một số bệnh có thể gây ra giảm hấp thu bởi niêm mạc, chúng thường được phân loại cùng nhau dưới thuật ngữ chung là sprue, hấp thu kém cũng có thể xảy ra khi các phần lớn của ruột non đã bị loại bỏ.
Cơ chế bệnh sinh của rối loạn tiêu hóa ruột non
Tình trạng thiếu bài tiết tuyến tụy thường xuyên xảy ra ở những người bị viêm tụy, khi ống tụy bị tắc do sỏi mật ở nhú Vater, hoặc sau khi đầu tụy bị cắt bỏ vì của bệnh ác tính.
Nguyên nhân cụ thể của loét dạ dày tá tràng
Các yếu tố nguy cơ của loét dạ dày tá tràng bao gồm hút thuốc lá, uống rượu, bởi rượu có xu hướng phá vỡ hàng rào niêm mạc; và uống thuốc aspirin và các NSAID khác.
Cơ chế bệnh sinh của loét dạ dày tá tràng
Nguyên nhân thông thường của loét đường tiêu hóa là sự mất cân bằng giữa tốc độ bài tiết dịch vị và các yếu tố bảo vệ bao gồm lớp hàng rào niêm mạc dạ dày - tá tràng và là sự trung hòa của acid dịch vị và dịch tá tràng.
Viêm dạ dày mãn tính có thể dẫn đến teo dạ dày và mất tuyến trong dạ dày
Việc mất khả năng tiết dịch vị trong teo niêm mạc dạ dày dẫn đến thiếu acid dịch vị, và đôi khi là thiếu máu ác tính.
Rối loạn dạ dày trong quá trình tiêu hóa
Viêm dạ dày thường gây ra bởi sự nhiễm khuẩn mạn tính niêm mạc dạ dày, tình trạng này có thể chữa khỏi hoàn toàn bới một liệu trình kháng sinh cường độ lớn.
Rối loạn nuốt và co thắt thực quản
Co thắt thực quản là tình trạng mà cơ thắt thực quản dưới không thể giãn khi nuốt. Hệ quả là thức ăn nuốt vào thực quản không thể đi tới dạ dày.
Phù não do tăng áp lực hoặc tổn thương thành mao mạch
Nguyên nhân thường gặp của phù não là do tăng áp lực trong mao mạch hoặc tổn thương thành mao mạch khiến dịch thấm qua thành mạch. Một nguyên nhân phổ biến là do chấn thương não, tình trạng tổn thương nhu mô não và các mao mạch.
Phân loại điếc: các bất thường về thính giác
Nếu ốc tai hoặc thần kinh thính giác bị phá hủy thì sẽ bị điếc vĩnh viễn. Nếu ốc tai và thần kinh thính giác vẫn còn nguyên vẹn mà hệ màng nhĩ - xương con bị phá hủy hoặc bị cứng khớp, sóng âm vẫn có thể truyền đến ốc tai bằng phương tiện dẫn truyền qua xương.
Điều tiết và độ mở của đồng tử: điều hòa tự động thần kinh tự động của mắt
Hệ giao cảm phân phối cho mắt bắt nguồn từ các tế bào sừng bên giữa trước ở đốt tủy ngực đầu tiên. Từ đó, các sợi giao cảm đi đến chuỗi hạch giao cảm và đi lên hạch cổ trên, nơi chúng xi náp với các neuron sau hạch.
Lác mắt: tổn thương điều hợp của mắt
Ở một số bệnh nhân lác, mắt thay thế trong việc chú ý đến đối tượng. Ở những bệnh nhân khác, một mắt đơn độc được sử dụng mọi lúc, và mắt kia trở nên bị ép và không bao giờ được sử dụng để nhìn chính xác.
Cử động vận nhãn: thần kinh chi phối cử động của mắt
Các cử động của mắt được phụ trách bởi ba nhóm cơ: cơ thẳng ngoài và cơ thẳng trong, cơ thẳng trên và cơ thẳng dưới, và cơ chéo trên và cơ chéo dưới.
Vỏ não thị giác sơ cấp: hậu quả của sự loại bỏ vỏ não
Để chẩn đoán mù ở các vị trí cụ thể của võng mạc, một bảng ghi lại sự đánh giá thị trường của mỗi mắt bằng một quá trình gọi là đo thị trường (perimetry).
Điều chỉnh tật khúc xạ bằng kính áp tròng và đục thể thủy tinh
Kính áp tròng có một vài ưu điểm và ngoài ra còn có đặc điểm như kính chuyển động đồng thời với mắt, kính áp tròng sẽ ảnh hưởng một ít đến kích thước thật của vật khi nhìn qua kính.
Hiệu chỉnh loạn thị bằng kính trụ: sử dụng hai kính trụ với độ hội tụ khác nhau
Sau khi thử vài thấu kính cầu khác nhau trước mắt loạn thị, mỗi độ hội tụ của thấu kính làm hội tụ rõ nét một vài các thanh song song nhau nhưng sẽ không rõ một vài các thanh khác vuông góc với các thanh sắc nét đó.
Loạn thị: rối loạn độ hội tụ của mắt
Loạn thị là tình trạng độ hội tụ của mắt bị rối loạn gây nên sự khác nhau về khả năng hội tụ của mắt trên các mặt phẳng vuông góc với nhau.
Tật khúc xạ: cận thị và viễn thị
Một người thường chọn độ hội tụ của kính phân kì hay kính hội tụ cần thiết bằng “phương pháp thử” - đó là, đầu tiên, thử một kính có độ hội tụ bất kì sau đó tiếp tục thử kính khác.
Cơ chế sự điều tiết của mắt: cơ chế quang học của mắt
Sự co một trong hai loại cơ thể mi này đều làm giảm độ căng của dây treo, giảm lực kéo dây treo tác dụng vào bao thấu kính và làm thấu kính trở thành hình cầu - như trạng thái tự nhiên của bao xơ đàn hồi.
Kích thích Receptor nhiệt và truyền tín hiệu nhiệt trong hệ thần kinh
Lượng đầu mút tận cùng lạnh và nóng trong bất kì vùng bề mặt nào của cơ thể là không đáng kể, rất khó để đánh giá sự thay đổi nhiệt độ khi một vùng da nhỏ bị kích thích.
Cảm giác nhiệt: Receptor và sự hưng phấn của chúng
Những receptor nóng và lạnh nằm ngay dưới da ở những điểm tách biệt riêng rẽ. Hầu hết các vùng của cơ thể, các điểm lạnh gấp 3 đến 10 lần điểm nóng, và những vùng khác nhau thì có số điểm khác nhau.
Đau đầu ngoài sọ: đau đầu do mắt và mũi
Sự căng thẳng cảm xúc thường làm co nhiều cơ của đầu, đặc biệt là cơ gắn vào da đầu và cơ cổ gắn với chẩm, trở nên co cứng, và nó được cho rằng cơ chế này là một trong những nguyên nhân thông thường của đau đầu.
Đau đầu nguồn gốc trong sọ: các thể đau đầu trong sọ
Mô não hầu như hoàn toàn không nhạy cảm với đau. Thậm chi khi cắt hoặc khi kích thích điện những vùng nhạy cảm của vỏ não chỉ thỉnh thoảng gây đau.
Hội chứng Brown Sequard: liệt vận động cùng bên tổn thương
Hội chứng Brown - Séquard gây những hệ quả có thể dự đoán được nhờ vào kiến thức về chức năng các bó trong tủy sống. Theo đó, toàn bộ chức năng vận động đều bị ngăn chặn ở bên cùng phía với tổn thương.
Cơn đau khác thường trên lâm sàng: những cảm giác bản thể
Nhiều bệnh của cơ thể gây đau. Hơn nữa khả năng chẩn đoán những bệnh khác nhau phụ thuộc rất lớn vào sự hiểu biết của bác sĩ lâm sàng về những đặc tính khác nhau của đau.
Xác định vị trí đau của tạng: đường dẫn truyền đau tạng và đau thành
Cảm giác đau từ các tạng khác nhau thường khó xác định rõ vị trí. Thứ nhất, não không nhận thức được về sự hiện diện của các cơ quan. Thứ hai, cảm giác từ ổ bụng và lồng ngực được dẫn truyền lên hệ thần kinh trung ương qua hai con đường:
Đau tạng: cơ chế và đặc điểm phân biệt với cơn đau từ bề mặt da
Bất kỳ kích thích nào gây hưng phấn những đầu tận sợi dẫn truyền đau trong vùng mơ hồ của tạng cũng có thể tạo ra một cơn đau tạng.
Đau quy chiếu: cảm nhận đau xuất phát từ mô cơ thể
Những sợi thần kinh dẫn truyền cảm giác đau từ các tạng có vị trí tiếp nối synapse trong tủy sống trên cùng một neuron thứ 2 (1 và 2) mà cũng nhận tín hiệu đau từ da.
Hệ thống Opiate của não: Endorphins và Enkephalins
Hệ thống opiate của não vẫn chưa được hiểu biết thấu đáo, hoạt động của hệ thống vô cảm thông qua tín hiệu thần kinh vào chất xám quanh cống não và vùng quanh não thất.
Ức chế (vô cảm) đau: hệ thống trong não và tủy sống
Mức độ mà con người phản ứng với cơn đau thì vô cùng đa dạng. Đây chủ yếu là kết quả của khả năng tự thân kiểm soát tín hiệu đau trong hệ thần kinh bằng cách hoạt hóa hệ thống ức chế đau, gọi là hệ thống vô cảm (analgesia system).
Bó gai đồi thị cũ và mới: hai con đường dẫn truyền đau trong tủy sống và thân não
Khi vào tủy sống, tín hiệu đau có hai con đường đến não, qua (1) bó gai đồi thì mới và (2) bó gai đồi thị cũ. Con đường dẫn truyền cảm giác đau chậm trong bó gai đồi thị cũ phần lớn sẽ tận cùng trong thân não.
Dẫn truyền đau: con đường kép trong hệ thần kinh trung ương
Receptor đau là các đầu mút tận cùng tự do, nhưng các đầu tận cùng này sử dụng hai đường để dẫn truyền các dấu hiệu đau trong hệ thần kinh trung ương. Hai đường tương đương với hai kiểu đau: đường đau nhanh và đường đau chậm.
Kích thích gây đau: phá hủy mô đạt mức đau
Trung bình một người bắt đầu cảm thấy đau khi da bị nóng trên 45 độ C. Đây cũng là nhiệt độ mà mô bắt đầu bị phá hủy bởi tác nhân nhiệt; thực tế là, mô thậm chí bị hủy hoại nếu nhiệt độ duy trì trên mức này.
Receptor đau: sự kích thích đầu tận cùng tự do của dây thần kinh
Các receptor đau trong da và trong các mô khác là các đầu tận cùng tự do của các dây thần kinh. Chúng có nhiều trên bề mặt da cũng như trong các nội tạng, như màng xương, thành động mạch, màng khớp, liềm đại não và lều tiểu não trong vòm sọ.
Phân loại và đặc điểm của đau: đau nhanh và đau chậm
Đau được phân thành hai loại chính: đau nhanh và đau chậm. Đau nhanh được cảm nhận thấy trong vòng khoảng 0.1 giây sau khi một kích thích đau được gây ra, trong khi đau chậm bắt đầu chỉ sau 1 giây hoặc hơn.
Khuếch tán của màng hô hấp: công xuất khuếch tán O2 và CO2 và tỷ lệ thông khí tưới máu
Một số vùng của phổi có sự lưu thông khí nhưng không có sự lưu thông máu và ngược lại. Chỉ cần 1 trong các điều kiện đó, trao đổi khí qua màng hô hấp khó khăn nghiêm trọng và người đó có thể suy hô hấp nặng.
Dịch trong khoang màng phổi: áp lực âm giữ cho phổi nở và lượng dịch màng phổi
Khi dịch nhiều hơn đủ để bắt đầu chảy trong khoang màng phổi thì các dịch dư thừa bị bơm đi bằng cách mở trực tiếp mạch bạch huyết từ khoang màng phổi vào trung thất, trên bề mặt cơ hoành và xung quanh màng phổi thành.
Động lực học của mao mạch phổi: trao đổi dịch mao mạch và động lực học dịch kẽ phổi
Phù phổi xảy ra cùng cách phù nề xảy ra ở những nơi khác trong cơ thể. Bất kì yếu tố làm tăng lọc dịch lỏng ra khỏi mao mạch phổi hoặc cản trở chức năng bạch huyết phổi và gây ra tăng áp lực lọc phổi kẽ từ âm sang dương.
Thể tích máu của phổi: thể tích ở trạng thái bình thường và bệnh lý
Theo những tình trạng sinh lý và bệnh lý, số lượng máu trong phổi có thể khác nhau từ ít nhất một nửa bình thường lên đến gấp đôi bình thường. Khi thở dốc rất mạnh, tạo áp lực cao trong phổi, 250 ml máu có thể ra khỏi tuần hoàn phổi vào tuần hoàn toàn thân.
Khả năng giãn nở của phổi: ảnh hưởng của lồng ngực
Lồng ngực có khả năng đàn hồi và dẻo, tương tự như phổi, thậm chí nếu phổi không hiện diện trong ngực, cơ hỗ trợ sẽ vẫn giúp lồng ngực giãn nở.
Khí ra vào phổi: áp lực gây ra sự chuyển động của không khí
Áp suất màng phổi là áp lực của dịch trong khoang mỏng giữa màng phổi lá tạng và màng phổi lá thành. Áp lực này bình thường hút nhẹ hay áp lực âm nhẹ.
Giãn nở và co phổi: sự tham gia của các cơ hô hấp
Trong kì hít vào, cơ hoành co làm kéo bề mặt phần dưới phổi xuống. Sau đó, kì thở ra, với cơ hoành giãn, phổi đàn hồi, thành ngực, sự nén các tạng bụng làm tống không khí ra ngoài.
Đông máu cầm máu: các xét nghiệm sử dụng trong lâm sàng
Máu lấy từ bệnh nhân ngay lập tức hòa trộn với oxalat nên không xảy ra quá trình chuyển hóa prothrombin thành thrombin. Sau đó, một lượng lớn ion calci và yếu tố mô nhanh chóng được hòa trộn với máu có oxalat.
Chống đông: các chất sử dụng ngoài cơ thể
Bất kì chất nào làm mất đi dạng ion của calci máu đều có thể ngăn ngừa quá trình đông máu. Ion citrat tích điện âm là rất phù hợp và thường được hòa trộn với máu ở dạng natri citrat, amoni citrat hoặc kali citrat.
Chống đông: những chất dùng trong lâm sàng
Trong một số trường hợp cần kìm hãm quá trình đông máu. Có nhiều chất có tác dụng chống đông trong đó hay dùng nhất là heparin và coumarin.
Đông máu nội mạch rải rác: tắc nghẽn mạch máu nhỏ ở ngoại vi
Sự tắc nghẽn các mạch máu nhỏ ngoại vi sẽ ngăn cản mô nhận oxy và các chất dinh dưỡng khác, điều này sẽ dẫn đến hoặc làm nặng thêm tình trạng shock tuần hoàn.
Huyết khối: tại tĩnh mạch đùi và động mạch phổi
Cục máu đông thường phát triển theo hướng dòng máu chảy chậm trong tĩnh mạch, đôi khi theo toàn bộ chiều dài tĩnh mạch chi dưới và thậm chí phát triển lên đến tĩnh mạch chậu chung và tĩnh mạch chủ dưới.
Huyết khối: nguy cơ gây tắc mạch nghiêm trọng
Nguyên nhân tạo nên huyết khối thường là bề mặt nội mô của mạch máu xù xì có thể gây ra bởi xơ vữa động mạch, nhiễm trùng hay chấn thương và tốc độ chảy rất chậm của máu trong lòng mạch.
Chảy máu qúa mức: do thiếu các yếu tố đông máu
Chảy máu quá mức có thể từ sự thiếu bất kì yếu tố đông máu nào. Có ba thể hay gặp nhất sẽ được nói đến ở đây đó là: (1) thiếu vitamin K, (2) hemophila và (3) giảm tiểu cầu.
Tan cục máu đông: plasmin làm tiêu fibrin và chất chống đông
Khi cục máu đông được tạo thành, có một lượng lớn plasminogen bị giam giữ trong cục máu đông với các protein huyết tương khác. Nếu chúng không được hoạt hóa thì sẽ không tạo thành plasmin và làm tan cục máu đông.
Hoạt hóa prothrombin: khởi đầu quá trình đông máu
Hầu hết các yếu tố đông máu được đánh số thứ tự La Mã. Khi muốn kí hiệu dạng hoạt hóa sẽ thêm chữ “h” nhỏ đằng sau số La Mã, ví dụ như yếu tố VIIh là dạng hoạt hóa của yếu tố VII.
Quá trình tạo cục máu đông: điều hòa ngược dương tính
Khi đã có một lượng thrombin nhất định được tạo thành, sẽ có một điều hòa ngược dương tính tạo nên càng nhiều cục máu đông và thrombin. Do đó, cục máu đông tiếp tục phát triển cho đến khi máu ngừng chảy.
Chuyển hóa fibrinogen thành fibrin: hình thành cục máu đông
Cục máu đông là một mạng lưới sợi fibrin chạy theo mọi hướng và giam giữ các tế bào máu, tiểu cầu và huyết tương. Các sợi fibrin cũng gắn với bề mặt mạch máu bị tổn thương.
Chuyển hóa prothrombin thành thrombin: cơ chế đông máu cầm máu
Nếu gan không sản xuất được prothrombin thì nồng độ prothrombin trong huyết tương có thể hạ xuống quá thấp, không đáp ứng nhu cầu sử dụng cho quá trình đông máu.
Cơ chế đông máu: chất chống đông và chất đông máu
Khi mạch máu bị tổn thương, chất đông máu trong vùng mô tổn thương sẽ được hoạt hóa và ưu thế hơn các chất chống đông, từ đó hỉnh thành cục máu đông.
Các giai đoạn cầm máu: ngăn mất máu khi mạch máu bị tổn thương
Cơ chế tạo nút tiểu cầu cực kì quan trọng để sửa chữa hàng ngàn lỗ tổn thương xảy ra hàng ngày ở các mạch máu rất nhỏ, như trong quá trình tạo lớp tế bào nội mô mới sẽ xuất hiện nhiều lỗ tổn thương như thế.
Hệ nhóm máu ABO và kháng thể trong huyết thanh
Khi đứa trẻ ra đời, nồng độ kháng thể gần như bằng 0. Ở giai đoạn 2 đến 8 tháng, đứa trẻ bắt đầu sản xuất ra kháng thể và nồng độ kháng thể đạt mức tối đa ở giai đoạn 8 đến 10 tuổi, rồi giảm dần trong những năm sau đó.
Ghép mô và cơ quan: phản ứng miễn dịch trong cấy ghép mô
Một số mô khác nhau và cơ quan đã được cấy ghép (hoặc nghiên cứu, hoặc thực nghiệm, điều trị) từ người này sang người khác là: da, thận, tim, gan, mô tuyến, tuỷ xương, phổi.
Hậu quả của truyền nhầm nhóm máu không hòa hợp
Tất cả các phản ứng truyền máu cuối cùng sẽ gây tan máu trực tiếp hoặc tán huyết. Các hemoglobin được giải phóng từ hồng cầu bị phá huỷ sẽ được chuyển đổi bởi các đại thực bào thành bilirubin và sau đó sẽ được bài tiết qua gan mật.
Tan máu tăng hồng cầu non ở trẻ sơ sinh
Các mô tạo máu của trẻ sơ sinh sản xuất máu thay thế các tế bào máu đã phá huỷ. Gan và lách trở nên lớn hơn và sản xuất hồng cầu giống như đã làm khi còn trong giai đoạn giữa của thai kì.
Hệ thống nhóm máu Rh và đáp ứng miễn dịch
Khi truyền máu Rh+ cho người có máu Rh- thì người Rh- sẽ sản xuất kháng thể anti-Rh. Sự tạo thành kháng thể anti-Rh diễn ra rất chậm, khoảng 2 đến 4 tháng sau nồng độ kháng thể mới đạt mức tối đa.
Phản ứng trong truyền máu và cách xác định nhóm máu: quá trình ngưng kết
Thỉnh thoảng, khi truyền máu không hoà hợp, có thể gây ra sự tiêu máu trực tiếp. Trong trường hợp này, kháng thể li giải hồng cầu bằng cách kích thích hệ thống bổ thể, tiết ra enzim phân giải protein ở màng tê bào.
Hệ nhóm máu ABO và kháng nguyên trên màng hồng cầu
Trên màng hồng cầu, người ta tìm thấy khoảng 30 kháng nguyên thường gặp và hàng trăm kháng nguyên khác. Các kháng nguyên này đều có phản ứng kháng nguyên kháng thể.
Loại tế bào lympho T: chức năng khác nhau của chúng
Lympho T helper, tính đến nay, là tế bào có số lượng nhiều nhất trong các loại lympho bào T, các lympho T helper có chức năng giúp đỡ các hoạt động của hệ miễn dịch.
Đặc tính của lympho T: hoạt hóa tế bào T và miễn dịch trung gian tế bào
Tế bào T đi vào tuần hoàn và được phân bố khắp cơ thể, đi qua thành mao mạch vào các khoảng gian bào, trở lại vào bạch huyết và máu một lần nữa, và tuần hoàn một lần nữa và một lần nữa trên khắp cơ thể.
Hệ thống bổ thể và hoạt động của kháng thể
Khi một kháng thể liên kết với một kháng nguyên, một vị trí phản ứng đặc hiệu trên của kháng thể bị phát hiện, hoặc hoạt hóa, và gắn trực tiếp với phân tử C1 của hệ thống bổ thể.
Tính đặc hiệu của tế bào lympho B: miễn dịch dịch thể và kháng thể
Tế bào lympho B đặc hiệu ngay lập tức phóng đại kháng nguyên và giao cho sự xuất hiện của nguyên bào lympho. Một số nguyên bào Lympho đẩy mạnh biệt hóa để tạo thành tiền tương bào, đó là tiền chất của tương bào.
Nguồn gốc của các dòng lympho: đề kháng của cơ thể trong nhiễm khuẩn
Đối với mỗi chức năng của T hoặc B được hình thành cuối cùng, các mã cấu trúc gen chỉ cho một kháng nguyên đặc hiệu. Tế bào trưởng thành sau đó trở thành T và B tế bào đặc hiệu cao được nhân lên và lan ra cuối mô bạch huyết.
Tế bào lympho T và B: kháng thể đáp ứng đối với kháng nguyên cụ thể và vai trong các dòng lympho
Hàng triệu loại tế bào tiền lympho B và tế bào lympho T có khả năng hình thành các loại kháng thể hoặc tế bào T đặc hiệu cao đã được lưu trữ trong các mô bạch huyết, được giải thích sớm hơn.
Tế bào lympho T và B kích hoạt miễn dịch trung gian tế bào và miễn dịch dịch thể
Mặc dù tất cả các tế bào bạch huyết trong cơ thể có nguồn gốc từ tế bào gốc tế bào tiền lympho của phôi thai, các tế bào gốc có khả năng hình thành trực tiếp hoặc hoạt hóa tế bào lympho T hoặc các kháng thể.
Miễn dịch thu được (thích ứng): đề kháng của cơ thể trong nhiễm khuẩn
Miễn dịch thu được là do một hệ thống miễn dịch đặc biệt hình thành kháng thể và hoặc hoạt hóa tế bào lympho tấn công và tiêu diệt các vi sinh vật xâm lấn cụ thể hoặc độc tố.
Miễn dịch và dị ứng: đề kháng của cơ thể trong nhiễm khuẩn
Miễn dịch bẩm sinh làm cho cơ thể con người đề kháng các bệnh như một số bệnh nhiễm virus bại liệt của động vật, bệnh tả heo, gia súc bệnh dịch, và bệnh distemper.
Ảnh hưởng của Leukemia trên cơ thể: di căn các tế bào leukemia
Ảnh hưởng thường gặp trong leukemia là phát triển sự nhiễm khuẩn, thiếu máu nặng, thiếu tiểu cầu. Các ảnh hưởng này chủ yếu dẫn đến từ sự thay thế các bạch cầu bình thường bằng các tế bào leukemia không có chức năng.
Leukemia: tăng số lượng bạch cầu bất thường
Hai loại Leukemia thông thường: leukemia thể lympho gây ra bởi sự quá sản của bạch cầu lympho, thường bắt đầu trong một hạch lympho hoặc một mô lympho khác rồi lan ra các vùng khác của cơ thể.
Giảm bạch cầu: giảm bảo vệ cơ thể chống lại nhiều vi khuẩn
Trong 2 ngày sau khi tủy xương dừng sản xuất bạch cầu, loét có thể xuất hiện ở miệng và ruột già hoặc một số người nhiễm khuẩn hô hấp nặng có thể tiến triển. Vi khuẩn từ vết loét nhanh chóng xâm nhập vào mô và máu.
Bạch cầu ưa base (bạch cầu ái kiểm): vai trò quan trọng trong phản ứng dị ứng
Dưỡng bào và bạch cầu ái kiềm đóng một vai trò quan trọng trong nhiều loại phản ứng dị ứng bởi lọai kháng thể gây ra phản ứng dị ứng, IgE có xu hướng đặc biệt gắn với dưỡng bào và bạch cầu ái kiềm.
Bạch cầu ưa acid (bạch cầu ái toan): chống lại nhiễm kí sinh trùng và dị ứng
Bạch cầu ái toan cũng có xu hướng đặc biệt tập trung nhiều trong các mô có phản ứng dị ứng, như trong các mô quanh phế quản ở người bị hen phế quản và trong da sau khi có phản ứng dị ứng da.
Quá trình điều hòa ngược các đáp ứng của đại thực bào và bạch cầu đa nhân trung tính
Khi bạch cầu hạt trung tính và đại thực bào nuốt phần lớn vi khuẩn và mô hoại tử, về cơ bản thì tất cả bạch cầu hạt trung tính và phần lớn đại thực bào cuối cùng sẽ chết.
Viêm nhiễm: sự đáp ứng của đại thực bào và bạch cầu hạt trung tính
Đại thực bào có thể thực bào nhiều vi khuẩn hơn (khoảng gấp 5 lần) và các phần tử lớn hơn, bao gồm cả bạch cầu hạt trung tính. Đại thực bào cũng đóng vai trò quan trọng trong việc khởi động sản xuất kháng thể.
Quá trình viêm: vai trò của bạch cầu hạt trung tính và dại thực bào
Viêm đặc trưng bởi sự giãn rộng của mạch tại chỗ, gây tăng lưu lượng máu tại chỗ; tăng tính thấm của mao mạch, cho phép rò rỉ một lượng lớn dịch vào khoảng kẽ; thường đông tụ dịch ở khoảng kẽ.
Hệ thống mono đại thực bào/ hệ thống võng nội mô
Tổ hợp toàn bộ bạch cầu mono, đại thực bào di động, đại thực bào mô cố định, và một vài tế bào nội mô chuyên biệt trong tủy xương, lách, và hạch lympho được gọi là hệ thống võng nội mô.
Sự thực bào: chức năng của bạch cầu hạt trung tính và đại thực bào
Ngoài việc tiêu hóa vi khuẩn ăn vào trong phagosome thì bạch cầu hạt trung tính và đại thực bào còn chứa các tác nhân diệt khuẩn giết được hầu hết vi khuẩn kể cả khi enzym của lysosome không tiêu hóa được chúng.
Bạch cầu đa nhân trung tính và đại thực bào chống lại nhiễm khuẩn
Cả bạch cầu hạt trung tính và đại thực bào có thể di chuyển trong mô bằng chuyển động kiểu amip. Vài tế bào di chuyển với tốc độ nhanh khoảng 40 µm/ph, một khoảng cách lớn so với chiều dai cơ thể chúng mỗi phút.
Đời sống của bạch cầu: thời gian trong máu tuần hoàn và trong mô
Đời sống bạch cầu sau khi rời khỏi tủy xương thường là 4-8h trong máu tuần hoàn và khoảng 4-5 ngày trong các mô cần chúng. Trong các nhiễm khuẩn nghiêm trọng ở mô, đời sống thường bị rút ngắn chỉ còn vài giờ.
Sự hình thành bạch cầu: quá trình hình thành trong tủy xương
Bạch cầu được hình thành trong tủy xương được dự trữ trong tủy xương đến khi chúng cần thiết phải đi vào hệ tuần hoàn. Sau đó, khi có nhu cầu, các yếu tố khác nhau làm cho chúng được giải phóng.
Các loại tế bào bạch cầu: sáu loại bạch cầu bình thường có mặt
Sáu loại bạch cầu bình thường có mặt trong máu: bạch cầu đa nhân trung tính, bạch cầu đa nhân ưa acid, bạch cầu đa nhân ưa base, tế bào mono, lympho bào, và đôi khi có tương bào.
Đa hồng cầu: ảnh hưởng đến chức năng hệ tuần hoàn
Trong đa hồng cầu, số lượng máu ở đám rối này được tăng lên rất nhiều. Hơn nữa, do máu chảy chậm chạp qua các mao mạch da trước khi vào đám rối tĩnh mạch, mang đến một lượng hemoglobin khử lớn hơn bình thường.
Đa hồng cầu: tăng số lượng hồng cầu và hematocrit
Các nguyên bào không ngừng sản xuất hồng cầu khi đã đủ lượng hồng cầu. Điều này làm cho tăng quá mức sản xuất hồng cầu giống như trong ung thư vú sản xuất dư thừa của một loại tế bào vú nào đó.
Thiếu máu: ảnh hưởng lên chức năng hệ tuần hoàn
Tăng cung lượng tim ở những người bị thiếu máu một phần bù đắp sự thiếu oxygen do thiếu máu vì mặc dù mỗi số lượng đơn vị máu chỉ mang một lượng nhỏ khí oxy, dòng máu có thể tăng đủ một lượng gần như bình thường của oxy cho các mô.
Thiếu máu: giảm hồng cầu hoặc hemoglobin trong các tế bào
Khi mất máu mãn tính xảy ra, một người thường không thể hấp thụ chất sắt từ ruột để tạo thành hemoglobin nhanh như nó bị mất. Có nhiều hồng cầu nhỏ hơn bình thường và có quá ít hemoglobin bên trong, làm tăng tế bào nhỏ và thiếu máu nhược sắc.
Chuyển hóa sắt: tổng hợp hemoglobin
Khi hồng cầu bị phá hủy, các hemoglobin từ các tế bào này được đưa vào các tế bào monocytemacrophage. Sắt giải phóng và được lưu trữ chủ yếu trong ferritin được sử dụng khi cần thiết cho sự hình thành của hemoglobin mới.
Tổng hợp hemoglobin: gắn kết ô xy và thải trừ CO2
Hemoglobin là có khả năng gắn không bền và thuận nghịch với phân tử oxi. Khả năng này liên quan đến hô hấp bởi vì chức năng cơ bản của hemoglobin là gắn với oxi tại phổi và giải phóng chúng tại mao mạch mô ngoại vi.
Hồng cầu: sản sinh biệt hóa và tổng hợp
Hầu hết hồng cầu được sản xuất tại các xương có màng như xương cột sống, xương ức, các xương sườn và các xương chậu. Thậm chí, các xương này cũng giảm sản xuất khi tuổi tăng lên.
Hồng cầu máu: nồng độ hình dạng kích thước và chức năng
Các tế bào hồng cầu có chức năng khác ngoài vận chuyển hemoglobin, nó chứa một lượng lớn carbonyc anhydrase, một enzyme xúc tác cho phản ứng thuận ngịch giữa CO2 và nước tạo ra carbonic acid (H2CO3), làm tăng tốc độ phản ứng.
Điều trị suy thận: ghép thận hoặc lọc máu với thận nhân tạo
Lọc máu không thể duy trì hoàn toàn bình thường các thành phần dịch cơ thể và không thể thay thế hoàn toàn các chức năng phức tạp của thận, sức khỏe của bệnh nhân vẫn bị suy giảm đáng kể.
Bệnh thận mạn: hoạt động của các nephron chức năng
Một phần của sự đáp ứng này xảy ra do tăng lượng máu đến và tăng mức loch cầu thận ở mỗi nephron còn lại, do sự phì đại của các mạch máu và cầu thận, cũng như thay đổi chức năng do giãn mạch.
Protein niệu: tăng tính thấm cầu thận trong hội chứng thận hư
Nguyên nhân dẫn đến việc tăng mất protein qua nước tiểu là do sự tăng tính thấm của màng đáy cầu thận. Vì vậy, các bệnh gây tăng tính thấm màng đáy cầu thận có thể gây hội chứng thận hư.
Viêm thận kẽ mạn: nguyên nhân do tổn thương kẽ thận
Tổn thương kẽ thận do nguyên nhân nhiễm khuẩn được gọi là viêm thận-bể thận. Tình trạng nhiễm khuẩn có thể do nhiều loại vi khuẩn khác nhau nhưng thường gặp nhất là E.coli do nhiễm khuẩn ngược dòng từ đường hậu môn.
Viêm cầu thận mạn: nguyên nhân do tổn thương cầu thận
Viêm cầu thận mạn thường khởi phát với sự tăng lắng đọng các phức hợp kháng nguyên kháng thế ở màng đáy cầu thận. Viêm cầu thận cấp, số lượng bệnh nhân nhiễm liên cầu chỉ chiếm một phần nhỏ trong tổng số bệnh nhân bị viêm cầu thận mạn.
Bệnh thận mạn: nguyên nhân do mạch máu thận
Ngay cả ở những người khỏe mạnh không có tăng huyết áp hay đái tháo đường tiềm ẩn, lượng huyết tương qua thận và mức lọc cầu thận (GFR) sẽ giảm 40-50% khi đến tuổi 80.
Bilaxten: thuốc kháng histamin điều trị dị ứng
Bilastine là một chất đối kháng histamin không gây buồn ngủ, có tác dụng kéo dài, đối kháng chọn lọc trên thụ thể H1 ngoại vi và không có ái lực với thụ thể muscarinic. Bilastine ức chế các phản ứng mẩn ngứa, ban đỏ trên da do histamin trong vòng 24 giờ sau khi sử dụng một liều đơn.
Bệnh thận mạn: vòng xoắn bệnh lý dẫn đến bệnh thận giai đoạn cuối
Biện pháp hiệu quả nhất để làm chậm lại quá trình suy giảm chức năng thận này là giảm huyết áp động mạch và giảm áp lực ở cầu thận, đặc biệt bằng việc sử dụng các thuốc như ức chế men chuyển hoặc thuốc ức chế thụ thể angiotensin II.
Bệnh thận mạn tính: thường liên quan đến suy giảm chức năng thận không hồi phục
Nói chung, bệnh thận mạn, cũng giống như tổn thương thận cấp, có thể xảy ra do tổn thương khởi phát ở hệ mạch thận, cầu thận, ống thận, tổ chức kẽ thận hay đường niệu thấp.
Tổn thương thận cấp: các biến đổi sinh lý
Hầu hết các trường hợp tổn thương thận cấp nghiêm trọng đều xảy ra tình trạng vô niệu hoàn toàn. Bệnh nhân sẽ tử vong trong vòng 8-14 ngày, trừ khi chức năng thận được phục hồi hoặc sử dụng thận nhân tạo.
Tổn thương thận cấp sau thận: nguyên nhân do các bất thường đường tiết niệu dưới
Một số nguyên nhân gây ra tổn thương thận cấp sau thận bao gồm tắc nghẽn cả 2 bên niệu quản hoặc bể thận do sỏi lớn hoặc cục máu động, tắc nghẽn bàng quang, và tắc nghẽn niệu đạo.
Tổn thương thận cấp tại thận: nguyên nhân do các bất thường tại thận
Tổn thương thận cấp tại thận có thể chia thành các nhóm sau: tình trạng tổn thương các mao mạch cầu thận hoặc các mạch nhỏ của thận, tình trạng tổn thương biểu mô ống thận, và tình trạng gây tổn thương kẽ thận.
Tổn thương thận cấp trước thận: nguyên nhân do giảm lượng máu tới thận
Khi dòng máu tới thận giảm thấp hơn nhu cầu cơ bản, thường dưới 20-25% dòng máu tới thận bình thường, các tế bào thận trở nên thiếu oxy, và giảm hơn nữa lượng máu tới thận, nếu kéo dài, sẽ gây tổn thương.
Tổn thương thận cấp: nguyên nhân gây tổn thương
Nguyên nhân dẫn đến tổn thương thận cấp (AKI) có thể chia thành 3 nguyên nhân chính là tổn thương thận cấp trước thận, tổn thương thận cấp tại thận, và tổn thương thận cấp sau thận.
Bệnh thận: tổn thương thận cấp và bệnh thận mạn
Trong phạm vi 2 phân loại, có rất nhiều các bệnh thận cụ thể có thể ảnh hưởng đến các mạch máu thận, cầu thận, ống thận, kẽ thận, các bộ phận của đường tiết niệu bên ngoài thận bao gồm cả niệu quản và bàng quang.
Thuốc chẹn kênh natri: giảm tái hấp thu natri ở ống góp
Sự giảm hoạt động của bơm Natri-Kali-ATP làm giảm vận chuyển Kali vào trong tế bào và do đó làm giảm bài tiết Kali vào dịch trong lòng ống thận. Vì lí do này, thuốc chẹn kênh Natri còn được gọi là lợi tiểu giữ kali, và giảm tỷ lệ bài tiết kali ra nước tiểu.
Đối kháng thụ thể mineralocorticoid: giảm tái hấp thu natri và giản bài tiết kali của ống góp
Do các thuốc này cũng ức chế tác dụng của aldosterone trong việc làm tăng bài tiết kali, nên dẫn đến giảm bài tiết kali ra nước tiểu. Đối kháng thụ thể mineralocorticoid cũng làm kali từ các tế bào đi vào trong dịch ngoại bào.
Thuốc ức chế carbonic anhydrase: ức chế tái hấp thu NaHCO3 ở ống lượn gần
Do việc bài tiết ion hydro (H+) và tái hấp thu HCO3- ở ống lượn gần được thực hiện cùng nhau thông qua cơ chế đồng vận chuyển ngược chiều Na-H+ ở mặt trong màng, giảm tái hấp thu HCO3- cũng làm giảm tái hấp thu natri.
Lợi tiểu thiazide: ức chế tái hấp thu natri và clo ở phần đầu ống lượn xa
Trong điều kiện thuận lợi, các thuốc này có thể bài tiết thêm tối đa khoảng 5-10% lượng dịch lọc cầu thận vào nước tiểu, tương đương với lượng natri bình thường được tái hấp thu ở ống lượn xa.
Lợi tiểu quai: giảm tái hấp thu natri clo và kali ở đoạn phình to nhánh lên quai Henle
Bằng việc ức chế cơ chế đồng vận chuyển Natri-clokali ở mặt trong màng của quai Henle, thuốc lợi tiểu quai làm tăng đào thải ra nước tiểu: Natri, clo, kali, nước cũng như các chất điện giải khác.
Lợi tiểu thẩm thấu: tăng áp lực thẩm thấu lòng ống thận gây giảm hấp thu nước
Lượng lớn nước tiểu cũng được đào thải trong các bệnh liên quan đến sự dư thừa các chất hòa tan và không được tái hấp thu từ lòng ống. Ví dụ, trong bệnh đái tháo đường, lượng glucose được lọc vào trong ống thận vượt quá khả năng tái hấp thu glucose.
Thuốc lợi tiểu: các loại và cơ chế tác dụng
Tác dụng lâm sàng chủ yếu của các thuốc lợi tiểu là làm giảm lượng dịch ngoại bào, đặc biệt trong những bệnh có kèm theo phù và tăng huyết áp.
Toan gây giảm HCO3-/H+ trong dịch ống thận: cơ chế bù trừ của thận
Cả nhiễm toan hô hấp và chuyển hóa đều gây giảm tỉ lệ HCO3-/H+ trong dịch ống thận. Như một kết quả, sự quá mức H+ trong ống thận làm giảm tái hấp thu HCO3- và để lại thêm H+ có sẵn để kết hợp với bộ đệm tiết niệu NH4+ và HPO4--.
Điều chỉnh bài tiết H + ở ống thận
Những thay đổi về nồng độ K+ trong huyết tương cũng có thể ảnh hưởng đến sự tiết H+ của ông thận. Hạ kali máu kích thích và tăng kali máu ức chế H + bài tiết ở ống lượn gần.
Định lượng bài tiết acid base qua thận
Để cân bằng acid-base, lượng acid bài tiết thuần phải bằng lượng acid sản xuất không bay hơi trong cơ thể. Trong nhiễm toan, acid bài tiết thuần tăng rõ rệt, đặc biệt do tăng tiết NH4+, do đó loại bỏ acid ra khỏi máu.
Hệ thống đệm amoniac: bài tiết H + dư thừa và tạo HCO3 mới
Đệm amoniac (NH3) bài tiết ion hydro trong ống góp. Amoniac khuếch tán vào lòng ống, tại đây nó phản ứng với H + được tiết ra) để tạo thành NH4 +, sau đó được thải ra ngoài.
Hệ thống đệm photphat mang H + dư thừa vào nước tiểu và tạo ra HCO3− mới
Trong điều kiện bình thường, phần lớn các phosphate được tái hấp thu và chỉ khoảng 30-40 mEq/ngày dành cho đệm H+. Do đó, phần lớn các bộ đệm với H+ dư trong dịch toan ở ống thận xảy ra thông qua hệ đệm ammoniac.
Kết hợp của H+ dư thừa với đệm photphat và amoniac trong ống thận tạo ra HCO3-
Các bộ đệm quan trọng nhất là bộ đệm phosphate và bộ đệm ammoniac. Ngoài ra còn có có hệ thống đệm yếu khác như đệm urat và citrate nhưng ít quan trong hơn.
Bài tiết H + chủ động: trong các tế bào kẽ của ống lượn xa và ống góp
Mặc dù sự bài tiết H+ ở đoạn cuối ống lượn xa và ống góp chỉ chiếm khoảng 5% của tổng H+ bài tiết. Nhưng cơ chế này rất quan trọng trong việc acid hóa tối đa nước tiểu.
Trong ống thận: HCO3- được lọc sau đó tái hấp thu bởi sự tương tác với H+
Quá trình tái hấp thu này được khởi đầu bởi một phản ứng trong ống thận giữa HCO3- được lọc ra ở cầu thận và H+ được bài tiết bởi tế bào thành ống thận.
Phần đầu ống thận: H+ được bài tiết bởi sự hoạt hóa lần hai
Ống thận tái hấp thu HCO3- bằng cách kết hợp H+ với HCO3- thành acid carbonic, sau đó lại phân ly thành CO2 và nước. Ion Na, được tái hấp thu nhờ sự trao đổi với H+ được bài tiết.
Ống thận: sự bài thiết H+ và sự tái hấp thu HCO3-
Khoảng 80-90% HCO3- tái hấp thu (và H+ bài tiết) được thực hiện ở ống lượn gần, chỉ một số ít HCO3- xuống ống lượn xa và ống góp. Ở đoạn dày của nhánh lên quai Henle, khoảng 10% HCO3- nữa được tái hấp thu, và phần còn lại được hấp thu ở ống lượn xa và ống góp.
Thận: vai trò trong cân bằng acid base
Thận điều chỉnh nồng độ H+ của dịch ngoại bào qua 3 cơ chế chính. Bài tiết H+, Tái hấp thu và lọc HCO3-, sản xuất HCO3- mới. Tất cả các quá trình này, được hoàn thành bởi cơ chế bài tiết cơ bản.
Tăng nồng độ H+: làm tăng thông khí phế nang
Kiểm soát hô hấp không thể đưa nồng độ H+ hoàn toàn về bình thường trong trường hợp có một nguyên nhân mất cân bằng ngoài hệ hô hấp ảnh hưởng đến pH.
Tăng thông khí phổi: giảm nồng độ H+ dịch ngoại bào và làm tăng pH
Nếu chuyển hóa tạo CO2 vẫn không đổi, chỉ có các yếu tố ảnh hưởng đến pCO2 trong dịch ngoại bào là tốc độ thông khí ở phổi. Thông khí phế nang càng cao, pCO2 càng thấp.
CO2: phổi thải ra giúp cân bằng quá trình trao đổi
Nếu tốc độ chuyển hóa hình thành CO2 tăng, pCO2 cũng tăng theo. Tương tự nếu chuyển hóa giảm, pCO2 cũng giảm. Nếu tỷ lệ thông khí phổi tăng lên, CO2 được thải ra ngoài nhiều và pCO2 trong giảm dịch ngoại bào.
Bộ đệm Protein: điều chỉnh thăng bằng kiềm toan nội bào
Ngoài nồng độ cao trong tế bào, một yếu tố khác góp phần vào khả năng đệm của protein là pKs của nhiều hệ thống protein khá gần với pH nội bào.
Hệ thống đệm phosphat: điều chỉnh thăng bằng kiềm toan trong cơ thể
Hệ thống đệm phosphat có pK của 6.8, giá trị đó không xa pH bình thường trong dịch cơ thể là 7,4; điều này cho phép hệ thống đệm hoạt động gần tối đa.
Động lực học của hệ đệm bicarbonate trong thăng bằng kiềm toan
Nồng độ của H2CO3 không phân ly không thể đo bằng dung dịch bởi vì nó nhanh chóng phân ly thành CO2 và H2O hoặc H + và HCO3-. Tuy nhiên, lượng CO2 hòa tan trong máu là tỷ lệ thuận với số lượng của H2CO3 không phân ly.
Hệ thống đệm bicarbonate điều chỉnh kiềm toan trong cơ thể
Từ những phản ứng, ta có thể thấy rằng H+ từ axit mạnh HCl phản ứng với HCO3- tạo thành H2CO3 axit rất yếu, do đó bị phân huỷ tạo thành CO2 và H2O. CO2 dư thừa rất nhiều dẫn tới kích thích hô hấp, trong đó loại bỏ CO2 từ dịch ngoại bào.
Hệ thống đệm H+ trong dịch cơ thể
Tầm quan trọng của hệ thống đệm được thể hiện rõ khi nồng độ H+ thấp trong các dịch cơ thể và lượng tương đối lớn acid được sản xuất ra trong cơ thể.
Cơ chế điều hòa nồng độ H+: hệ thống đệm phổi thận
Khi có sự thay đổi nồng độ H+, các hệ thống đệm trong dịch cơ thể sẽ phản ứng ngay trong vòng vài giây để giảm thiểu sự thay đổi này. Hệ thống đệm không thể loại bỏ H+ hoặc thêm H+ cho cơ thể.
Nồng độ ion H+: các yếu tố chính ảnh hưởng đến acid base
Nồng độ H+ được quyết định bởi sự hoạt động của hầu hết các loại enzyme trong cơ thể. Do đó những thay đổi trong nồng độ H+ thể hiện hoạt động chức năng của tế bào và cơ quan trong cơ thể.
Xơ gan: giảm tổng hợp protein huyết tương ở gan và giữ natri ở thận
Khi dịch và protein bị mất khỏi tuần hoàn, các phản ứng của thận tương tự như các phản ứng được quan sát thấy trong các tình trạng khác liên quan đến giảm thể tích huyết tương.
Hội chứng thận hư: mất protein theo nước tiểu và giữ natri
Do nồng độ protein huyết tương giảm, áp suất thẩm thấu keo huyết tương giảm xuống mức thấp. Điều này khiến các mao mạch trên khắp cơ thể lọc một lượng lớn dịch vào các mô khác nhau, do đó gây ra phù nề và giảm thể tích huyết tương.
Tăng thể tích máu do tăng lưu lượng mạch máu
Trong thai kỳ, sức chứa mạch máu của tử cung, nhau thai và các cơ quan mở rộng khác của cơ thể người phụ nữ tăng lên thường xuyên làm tăng lượng máu từ 15 đến 25 phần trăm.
Bệnh tim: tăng khối lượng máu và khối lượng dịch ngoại bào
Nếu suy tim không quá nặng, sự gia tăng thể tích máu thường có thể đưa cung lượng tim trở lại và áp lực động mạch hầu như trở về bình thường và bài tiết natri cuối cùng sẽ tăng trở lại bình thường.
Lượng natri đưa vào cơ thể: các đáp ứng kiểm sát tổng hợp
Lượng natri cao ức chế hệ thống chống bài niệu và kích hoạt hệ thống bài niệu. Khi lượng natri tăng lên, lượng natri đầu ra ban đầu hơi chậm hơn lượng hấp thụ.
Peptide lợi niệu tâm nhĩ (ANP): vai trò trong việc kiểm soát bài tiết của thận
Những thay đổi về nồng độ ANP có thể giúp giảm thiểu những thay đổi về thể tích máu trong những đợt rối loạn khác nhau, chẳng hạn như lượng muối và nước tăng lên.
ADH: vai trò trong việc bài tiết nước qua thận
Nồng độ ADH cao không gây ra sự gia tăng lớn về thể tích dịch cơ thể hoặc áp lực động mạch, mặc dù nồng độ ADH cao có thể làm giảm nghiêm trọng nồng độ ion natri ngoại bào.
Aldosterone: vai trò trong việc kiểm soát bài tiết của thận
Trong trường hợp hoàn toàn không có aldosterone, tình trạng suy giảm thể tích có thể nghiêm trọng trừ khi người đó được phép ăn nhiều muối và uống nhiều nước để cân bằng lượng muối và nước trong nước tiểu tăng lên.
Angiotensin II: vai trò trong việc kiểm soát bài tiết của thận
Khi lượng natri giảm xuống dưới mức bình thường, nồng độ Angiotensin II tăng lên gây giữ natri và nước, đồng thời chống lại việc giảm huyết áp động mạch nếu không xảy ra.
Hệ thần kinh giao cảm kiểm soát bài tiết của thận: cơ quan thụ cảm động mạch và phản xạ áp suất
Sự giảm thể tích máu đủ lớn để làm giảm áp lực động mạch hệ thống, thì sự hoạt hóa hơn nữa của hệ thần kinh giao cảm xảy ra do sự giảm căng của các cơ quan thụ cảm động mạch nằm trong xoang động mạch cảnh và cung động mạch chủ.
Dịch ngoại bào: phân bố dịch giữa khoảng kẽ và mạch máu
Thể tích dịch ngoại bào và thể tích máu thường được kiểm soát đồng thời, nhưng số lượng phân phối dịch giữa kẽ và máu phụ thuộc vào các đặc tính vật lý của tuần hoàn và khoảng kẽ, cũng như động lực của quá trình trao đổi dịch qua các màng mao mạch.
Độ chính xác của thể tích máu và điều chỉnh dịch ngoại bào
Sự thay đổi nhỏ trong huyết áp gây ra sự thay đổi lớn về lượng nước tiểu. Những yếu tố này kết hợp với nhau để cung cấp phản hồi kiểm soát lượng máu hiệu quả.
Thận bài tiết natri và dịch: phản hồi điều chỉnh dịch cơ thể và áp suất động mạch
Trong quá trình thay đổi lượng natri và dịch, cơ chế phản hồi giúp duy trì cân bằng dịch và giảm thiểu những thay đổi về thể tích máu, thể tích dịch ngoại bào và áp suất động mạch.
Cân bằng natri và dịch trong cơ thể: tầm quan trọng của natri và áp lực bài niệu
Bài tiết áp lực đề cập đến tác động của huyết áp tăng lên để tăng bài tiết khối lượng nước tiểu, trong khi bài tiết natri áp lực đề cập đến sự gia tăng bài tiết natri xảy ra với huyết áp cao.
Bài tiết natri: điều chỉnh bằng mức lọc cầu thận hoặc tái hấp thu ở ống thận
Tái hấp thu ống và mức lọc cầu thận thường được điều chỉnh một cách chính xác, vì vậy sự bài tiết qua thận có thể khớp chính xác với lượng nước và chất điện giải.
Hấp thụ và bài tiết natri: được cân bằng trong trạng thái ổn định
Nếu rối loạn chức năng thận không quá nghiêm trọng, có thể đạt được cân bằng natri chủ yếu bằng cách điều chỉnh nội thận với những thay đổi tối thiểu về thể tích dịch ngoại bào hoặc các điều chỉnh toàn thân khác.
Kiểm soát dịch ngoại bào: các cơ chế của thận
Sự thay đổi lượng natri clorua trong dịch ngoại bào tương ứng với sự thay đổi tương tự lượng nước ngoại bào, và do đó duy trì nồng độ thẩm thấu và nồng độ natri tương đối ổn định.
Kiểm soát sự bài tiết magie qua thận và nồng độ ion magie ngoại bào
Điều chỉnh bài tiết magie được thực hiện chủ yếu bằng cách thay đổi tái hấp thu ở ống thận. Ống lượn gần thường chỉ tái hấp thu khoảng 25% lượng magie đã lọc.
Điều chỉnh bài tiết phốt phát của thận
Những thay đổi về khả năng tái hấp thu phosphat ở ống thận cũng có thể xảy ra trong các điều kiện khác nhau và ảnh hưởng đến sự bài tiết phosphat.
Kiểm soát sự bài tiết Canxi của thận
Tái hấp thu canxi tương tự như đối với natri, sự bài tiết canxi được điều chỉnh để đáp ứng nhu cầu của cơ thể, khi tăng lượng canxi ăn vào, cũng làm tăng bài tiết canxi qua thận. Canxi vừa được lọc vừa tái hấp thu ở thận nhưng không được bài tiết ra ngoài. Do đó, tốc độ bài tiết canxi qua thận...
Kiểm soát sự bài tiết canxi ở thận và nồng độ ion canxi ngoại bào
Đường tiêu hóa và các cơ chế điều hòa ảnh hưởng đến sự hấp thu và bài tiết canxi ở ruột đóng một vai trò quan trọng trong việc cân bằng canxi nội môi.
Các yếu tố chính điều chỉnh sự bài tiết kali của thận
Các yếu tố quan trọng nhất kích thích sự bài tiết kali của các tế bào chính bao gồm tăng nồng độ kali trong dịch ngoại bào, tăng aldosterone, và tăng tốc độ dòng chảy của ống thận.
Thận bài tiết kali: bởi tế bào chính của ống lượn xa và ống góp
Việc bài tiết kali từ máu vào lòng ống là một quá trình gồm hai bước, bắt đầu bằng sự hấp thu từ các kẽ vào trong tế bào nhờ bơm natri-kali ATPase ở màng tế bào bên.
Hấp thu và bài tiết kali qua thận
Sự thay đổi hàng ngày trong bài tiết kali được gây ra chủ yếu bởi những thay đổi trong bài tiết kali ở các ống ở lượn xa và ống góp. Các vị trí quan trọng nhất để điều hòa bài tiết kali là các tế bào chính của cuối ống lượn xa và ống góp.
Điều chỉnh phân phối kali trong cơ thể
Hấp thụ kali trong một bữa ăn nhiều rau và trái cây vào một thể tích dịch ngoại bào, sẽ làm tăng nồng độ kali trong huyết tương, hầu hết kali ăn vào sẽ nhanh chóng di chuyển vào các tế bào cho đến khi thận có thể loại bỏ lượng dư thừa.
Nồng độ kali: điều chỉnh nồng độ trong dịch ngoại bào và bài tiết
Duy trì sự cân bằng giữa lượng kali ăn vào và ra phụ thuộc chủ yếu vào sự bài tiết qua thận vì lượng bài tiết qua phân chỉ chiếm khoảng 5 đến 10 phần trăm lượng kali ăn vào.
Kiểm soát áp suất thẩm thấu và nồng độ natri: cơ chế osmoreceptor-ADH và cơ chế khát
Trong trường hợp không có các cơ chế ADH-khát, thì không có cơ chế feedback khác có khả năng điều chỉnh thỏa đáng nồng độ natri huyết tương và áp suất thẩm thấu.
Kiểm soát áp suất thẩm thấu và nồng độ natri: tầm quan trọng của sự khát nước
Nhiều yếu tố trong số các yếu tố tương tự nhau gây kích thích sự bài tiết ADH cũng làm tăng sự khát nước, nó được định nghĩa là ý thức rõ ràng sự mong muốn nước.
Kích thích tiết ADH: tầm quan trọng của độ thẩm thấu và phản xạ tim mạch
Với sự giảm thể tích máu, nồng độ ADH nhanh chóng tăng lên. Như vậy, với mức giảm nghiêm trọng về thể tích máu, các phản xạ tim mạch đóng một vai trò quan trọng trong việc kích thích sự bài tiết ADH.
Kích thích giải phóng ADH: do áp lực động mạch giảm và / hoặc thể tích máu giảm
Bất cứ khi nào huyết áp và lượng máu bị giảm, chẳng hạn như xảy ra trong xuất huyết, sự tăng tiết ADH dẫn đến tăng sự tái hấp thu dịch bởi thận, giúp khôi phục huyết áp và lượng máu về bình thường.
Tổng hợp ADH ở vùng dưới đồi và giải phóng từ thùy sau tuyến yên
Sự bài tiết ADH để đáp ứng với kích thích thẩm thấu là nhanh chóng, vì vậy nồng độ ADH huyết tương có thể tăng nhiều lần trong vòng vài phút, do đó cung cấp một phương thức thay đổi sự bài xuất nước qua thận của.
Áp suất thẩm thấu và nồng độ natri của cơ thể
Sự gia tăng áp suất thẩm thấu dịch ngoại bào làm cho các tế bào thần kinh đặc biệt gọi là các tế bào osmoreceptor, nằm ở phần trước vùng dưới đồi gần các nhân opraotic, co rút lại.
Cơ chế cô đặc nước tiểu: những thay đổi áp suất thẩm thấu ở các đoạn khác nhau của ống thận
Sự giảm cô đặc do urê ít được tái hấp thu vào tủy kẽ từ các ống góp khi nồng độ ADH thấp và thận hình thành một khối lượng lớn nước tiểu pha loãng.
Duy trì áp suất thẩm thấu cao vùng tủy thận: trao đổi ngược dòng trong recta vasa
Khi máu đi vào vùng tủy thận về phía nhú, nó dần dần trở nên cô đặc hơn, một phần do chất tan đi vào từ vùng kẽ và một phần là do sự mất nước vào vùng kẽ.
Hình thành nước tiểu cô đặc: ure góp phần tăng áp lực thẩm thấu vùng tủy thận
Nồng độ cao của urê trong dịch ống thận của ống góp vùng tủy trong làm cho urê khuếch tán ra khỏi ống thận đi vào dịch kẽ thận.
Bài tiết nước tiểu cô đặc: vai trò của ống lượn xa và ống góp
Bằng cách tái hấp thu càng nhiều nước có thể, thận tạo ra nước tiểu đậm đặc, bài xuất một lượng bình thường các chất tan trong nước tiểu trong khi đưa thêm nước trở lại dịch ngoại bào và bù đắp cho sự thiếu hụt nước trong cơ thể.
Chất tan giữ lại trong tủy thận: những điểm đặc biệt của quai Henle
Nước khuếch tán ra ngoài đầu dưới nhánh xuống quai Henle vào kẽ tủy và áp suất thẩm thấu dịch ống thận dần dần tăng lên khi nó chảy về phía chóp quai Henle.
Cơ chế hệ số nhân ngược dòng: tạo ra áp suất thẩm thấu cao vùng tủy thận
Khi nồng độ chất tan cao trong tủy thận đạt được, nó được duy trì bởi tính cân bằng giữa sự vào và thoát ra của các chất tan và nước trong tủy thận.
Bài tiết nước tiểu cô đặc: nồng độ ADH cao và áp suất thẩm thấu cao vùng tủy thận
Các ống góp xung quanh kẽ tủy thận thường có áp suất thẩm thấu cao, vì vậy khi nồng độ ADH cao, nước di chuyển qua màng tế bào ống thận bằng cách thẩm thấu vào kẽ thận.
Trọng lượng riêng của nước tiểu
Mối quan hệ giữa trọng lượng riêng và độ thẩm thấu thay đổi khi có một lượng đáng kể các đại phân tử trong nước tiểu, chẳng hạn như glucose, phương pháp cũ trong chẩn đoán xác định, hay một số thuốc kháng sinh.
Thận giữ nước bằng cách bài tiết nước tiểu cô đặc
Khả năng cô đặc tối đa của thận bắt buộc phải có bao nhiêu khối lượng nước tiểu phải được thải ra mỗi ngày khỏi cơ thể của các sản phẩm chất thải chuyển hóa và ion từ thức ăn.
Cơ chế thận bài tiết nước tiểu pha loãng
Qúa trình pha loãng đạt được bằng cách tái hấp thu các chất tan đến một mức độ lớn hơn so với nước, nhưng điều này chỉ xảy ra trong các phân đoạn nhất định của hệ thống ống thận.
Hormon chống bài niệu kiểm soát sự cô đặc nước tiểu
Khi độ thẩm thấu của các dịch cơ thể tăng trên bình thường, thùy sau tuyến yên tiết ra nhiều hơn ADH, điều đó làm tăng tính thấm nước của các ống lượn xa và ống góp.
Thận bài tiết nước dư thừa bằng cách hình thành nước tiểu loãng
Thận bình thường có một khả năng rất lớn để thay đổi tỷ lệ tương đối của các chất tan và nước trong nước tiểu để đáp ứng với những thách thức khác nhau.
Tái hấp thu và bài tiết của thận: tính từ sự thanh thải
Nếu lưu lượng thải một chất lớn hơn lưu lượng lọc chất đó, khi đó, lưu lượng bài tiết sẽ là tổng của lưu lượng lọc và bài tiết của ống thận.
Ước tính lưu lượng huyết tương qua thận: độ thanh thải PAH
Do mức lọc cầu thận mức lọc cầu thận chỉ chiếm khoảng 20% lưu lượng máu qua thận, một chất được thải trừ hoàn toàn ra khỏi huyết tương phải được bài tiết ở ống thận cũng như lọc ở cầu thận.
Ước tính mức lọc cầu thận: độ thanh thải và nồng độ creatinin huyết tương
Nếu như mức lọc cầu thận đột ngột giảm xuống còn 50% giá trị bình thường, thận sẽ không lọc hết và chỉ bài tiết một nửa lượn creatinine, gây lắng đọng creatinine trong cơ thể.
Ước tính mức lọc cầu thận: độ thanh thải inulin
Inulin không được sản xuất bởi cơ thể, được tìm thấy ở rễ một số loại thực vật và phải tiêm tĩnh mạch cho bệnh nhân để đo mức lọc cầu thận.
Đánh giá chức năng thận: sử dụng độ thanh thải
Độ thanh thải của một chất tượng trưng cho thể tích huyết tương cần thiết để cung cấp một lượng tương đương chất đó được bài tiết ra nước tiểu trong một đơn vị thời gian.
Tăng tái hấp thu natri ở ống thận: kích hoạt thần kinh giao cảm
Hoạt hóa hệ thần kinh giao cảm, nếu trầm trọng, có thể gây giảm sự bài tiết natri và nước do co mạch thận, làm giảm mức lọc cầu thận.
Nội tiết điều hòa tái hấp thu ở ống thận
Để giữ cho thể tích dịch cơ thể và nồng độ các chất tan ở mức ổn định, đòi hỏi thận phải bài tiết nước và các chất tan khác nhau ở các mức độ khác nhau, chất này độc lập với chất kia.
Ảnh hưởng của áp lực động động mạch đến lượng nước tiểu: bài niệu natri áp lực và bài niệu
Khi cơ chế tự điều hòa của mức lọc cầu thận bị suy giảm, thường xảy ra trong các bệnh thận, tăng áp lực động mạch sẽ làm tăng mức lọc cầu thận rất nhiều.
Lưu lượng dịch mao mạch và dịch mô kẽ trong thận
Hai yếu tố quyết định sự tái hấp thu ở mao mạch ống thận chịu ảnh hưởng trực tiếp của những thay đổi huyết động ở thận là áp suất thẩm thấu thủy tĩnh và chất keo của mao mạch ống thận.
Cân bằng cầu thận ống thận: tăng tái hấp thu để đáp ứng với sự gia tăng lưu lượng ống thận
Cân bằng giữa cầu thận và ống thận là hiện tượng tăng khả năng tái hấp thu tuyệt đối khi mức lọc cầu thận tăng, mặc dù phần trăm dịch lọc được tái hấp thu ở ống lượn gần vẫn giữ nguyên ở khoảng 65%.
Nồng độ của các chất hòa tan trong các đoạn ống thận
Thay đổi nồng độ của các chất qua các đoạn khác nhau của ống thận thống qua tỉ số giữa nồng độ huyết tương và ở dịch lọc.
Tái hấp thu của ống góp tủy thận
Các ống góp của tuỷ tích cực tái hấp thu natri và tiết ra các ion hydro và có thể thấm qua urê, được tái hấp thu trong các đoạn ống này. Sự tái hấp thu nước trong ống góp của tuỷ được kiểm soát bởi nồng độ của hormone chống bài niệu.
Tái hấp thu ở đoạn xa của ống lượn xa và ống góp phần vỏ
Tế bào chính tái hấp thu Natri và nước từ lòng ống và bài tiết ion Kali vào trong ống thận. Các tế bào kẽ thận loại A tái hấp thu ion Kali và bài tiết ion Hydro vào lòng ống.
Vận chuyển các chất ở ống lượn xa
Natri và clorua được vận chuyển từ lòng ống vào tế bào nhờ chất đồng vận chuyển bị ức chế bởi thuốc lợi tiểu thiazide.
Vận chuyển nước và các chất ở quai Henle của thận
Đoạn dày của ngành lên quai Henle hầu như không thấm nước. Do đó, hầu hết nước qua đoạn này vẫn ở lại trong lòng ống mặc dù có một lượng lớn chất tan được tái hấp thu.
Tái hấp thu ở ống lượn gần: tái hấp thu chủ động và thụ động
Ống lượn gần có công suất tái hấp thu lớn là do tế bào của nó có cấu tạo đặc biệt. Tế bào biểu mô ống lượn gần có khả năng trao đổi chất cao và lượng lớn ty thể hỗ trợ cho quá trình vận chuyển tích cực mạnh.
Tái hấp thu clorua, urê và các chất hòa tan khác ở thận bằng cách khuếch tán thụ động
Creatinine là một phân tử lớn hơn ure và hầu như không thấm qua màng tế bào ống thận. Do đó, creatinin lọc ở cầu thận gần như không được tái hấp thu, và do đó tất cả creatinin lọc ở cầu thận đều bài tiết ra nước tiểu.
Sự tái hấp thu nước ở thận: thụ động bằng thẩm thấu được kết hợp chủ yếu với sự tái hấp thu natri
Ở ống lượn gần, tính thấm nước luôn cao nên nước được tái hấp thu nhanh như chất tan. Ở quai Henle, tính thấm nước thấp, nên hầu như nước không được tái hấp thu mặc dù gradient thẩm thấu lớn.
Vận chuyển tích cực qua màng ống thận
Vận chuyển tích cực có thể di chuyển chất tan ngược chiều bậc thang điện hóa và đòi hỏi năng lượng sinh ra từ quá trình chuyển hóa.
Tái hấp thu ở ống thận: bao gồm các cơ chế thụ động và chủ động
Chất tan được vận chuyển qua tế bào bởi vận chuyển chủ động hoặc thụ động, hay giữa các tế bào bằng cách khuyếch tán. Nước được vận chuyển qua tế bào và giữa các tế bào ống thận bằng cách thẩm thấu.
Sự tái hấp thu ở ống thận: lớn về mặt định lượng và có tính chọn lọc cao
Đối với nhiều chất, tái hấp thu ở ống thận đóng một vai trò quan trọng hơn nhiều bài tiết trong việc xác định tỉ lệ bài tiết cuối cùng trong nước tiểu.
Cơ chế myogenic tự điều chỉnh lưu lượng máu qua thận và mức lọc cầu thận
Mặc dù cơ chế myogenic hoạt động ở hầu hết các tiểu động mạch đi khắp cơ thể, tầm quan trọng của nó trong lưu lượng máu thận và mức lọc cầu thận tự điều đã được đề cập.
Macula Densa natri clorua giảm gây ra sự giãn nở của các tiểu động mạch liên quan và tăng giải phóng Renin
Renin giải phóng từ các tế bào này sau đó có chức năng như một loại enzyme để tăng sự hình thành của angiotensin I, được chuyển thành angiotensin II.
Phản hồi cầu thận và tự động điều chỉnh mức lọc cầu thận
Phức hợp cầu thận bao gồm các tế bào điểm vàng ở phần ban đầu của ống lượn xa và các tế bào cạnh cầu thận trong thành của tiểu động mạch hướng tâm và tiểu động mạch ra.
Tự điều hòa mức lọc cầu thận để ngăn ngừa thay đổi bài tiết của thận
Những cơ chế kiểm soát đặc biệt, thay đổi huyết áp vẫn có những ảnh hưởng đáng kể về bài tiết nước và muối; này được gọi là nhiều áp lực tiểu hoặc bài niệu natri áp lực, và nó là rất quan trọng trong việc điều tiết lượng dịch cơ thể và huyết áp.
Tự điều chỉnh mức lọc cầu thận và lưu lượng máu qua thận
Mức lọc cầu thận bình thường vẫn tự động điều chỉnh (có nghĩa là, nó vẫn còn tương đối không đổi) bất chấp những biến động huyết áp đáng kể xảy ra trong quá trình hoạt động bình thường của một người.
Kiểm soát tuần hoàn thận của hormon và các chất hóa học
Trong trạng thái căng thẳng, chẳng hạn như sự suy giảm khối lượng hoặc sau khi phẫu thuật, các thuốc kháng viêm không steroid như aspirin, ức chế tổng hợp prostaglandin có thể gây ra giảm đáng kể mức lọc cầu thận.
Giảm mức lọc cầu thận: hoạt động của hệ thần kinh giao cảm mạnh
Tất cả mạch máu trong thận, gồm tiểu động mạch đến và đi, giàu phân bố các dây thần kinh của hệ thần kinh giao cảm. Thần kinh giao cảm hoạt động mạnh làm co tiểu động mạch thận và giảm dòng chảy qua thận và mức lọc cầu thận.
Yếu tố quyết định lưu lượng máu qua thận
Mặc dù thay đổi áp lực động mạch có ảnh hưởng lên dòng máu qua thận, thận có cơ chế tác động để duy trì dòng máu qua thận và mức lọc cầu thận cố định.
Lưu lượng máu qua thận và sự tiêu thụ ô xy
Trong mỗi gram trọng lượng cơ bản, thận bình thường tiêu thụ oxygen tốc độ gấp đôi so với não nhưng có gấp 7 lần dòng chảy của não.
Tăng mức lọc cầu thận: tăng áp suất thủy tĩnh mao mạch cầu thận
Áp suất thủy tĩnh cầu thận được xác định bởi ba biến số, mỗi biến số đều nằm trong tầm kiểm soát sinh lý, áp lực động mạch, sức cản của tiểu động mạch hướng tâm, và sức cản của tiểu động mạch.
Giảm mức lọc cầu thận: tăng áp suất thẩm thấu keo mao mạch cầu thận
Tăng áp suất keo huyết tương động mạch kéo theo tăng áp suất keo mao mạch cầu thận, quay trở lại làm giảm mức lọc cầu thận.
Giảm mức lọc cầu thận: tăng áp suất thủy tĩnh của khoang Bowman
Trong trạng thái bệnh nào đó liên quan đến cấu trúc đường tiểu, áp lực khoang Bowman’s có thể tăng rõ rệt, gây ra giảm trầm trọng mức lọc cầu thận.
Tăng mức lọc cầu thận: tăng hệ số lọc mao mạch cầu thận
Mặc dù tăng Kf kéo theo tăng mức lọc cầu thận và giảm Kf, làm giảm mức lọc cầu thận, nhưng thay đổi Kf hầu như chắc chắn không là cơ chế tiên phát cho việc điều chỉnh mức lọc cầu thận hàng ngày bình thường.
Tính mức lọc cầu thận (GFR): các lực gây ra quá trình lọc
Giá trị mức lọc cầu thận bình thường không đo được trực tiếp trên con người, chúng được ước lượng trên động vật như chó hay chuột. Dựa kết quả trên động vật, chúng ta có thể tin rằng chúng xấp xỉ trên con người.
Màng mao mạch cầu thận: bước đầu hình thành nước tiểu
Khả năng lọc của chất tan tỉ lệ ngịch với kích thước của chúng. Màng mao mạch cầu thận dày hơn các mao mạch khác, nhưng có nhiều lỗ nhỏ hơn và do đó lọc dịch tốc độ cao.
Mức lọc cầu thận bằng hai mươi phần trăm lưu lượng máu qua thận
Mức lọc cầu thận được quyết định bởi cân bằng thủy tĩnh và áp suất keo qua màng mao mạch hệ số lọc cầu thận, phụ thuộc tính thấm mao mạch cầu thận và diện tích.
Thành phần của dịch lọc cầu thận
Dịch lọc cầu thận gồm chủ yếu muối và các phân tử hữu cơ, tương tự như trong huyết thanh. Trừ một số trường hợp ngoại lệ đó là các phân tử có trọng lượng phân tử thấp như Canxi và acid béo không được lọc một cách tự do.
Các chất qua hệ tiết niệu: lọc, tái hấp thu và bài tiết
Một số chất dinh dưỡng nhất định, chẳng hạn như axit amin và glucose, được tái hấp thu hoàn toàn từ ống thận và không xuất hiện trong nước tiểu mặc dù một lượng lớn được lọc bởi mao mạch cầu thận.
Hình thành nước tiểu: lọc ở cầu thận tái hấp thu ở ống thận và sự bài tiết ở ống thận
Khi dịch được lọc ra khỏi bao Bowman và đi qua các ống, nó được biến đổi bằng cách tái hấp thu nước và các chất hòa tan cụ thể trở lại máu hoặc bằng cách tiết các chất khác từ các mao mạch phúc mạc vào ống.
Phản xạ tiểu tiện khi bàng quang đầy
Khi bàng quang chỉ được lấp đầy một phần, những cơn co thắt cơ này thường giãn ra một cách tự nhiên sau một phần của phút, các cơ ức chế ngừng co bóp và áp lực giảm trở lại mức ban đầu.
Vận chuyển nước tiểu từ thận qua niệu quản vào bàng quang
Thành bàng quang có xu hướng nén niệu quản, do đó ngăn chặn dòng chảy ngược (trào ngược) nước tiểu từ bàng quang khi áp lực tích tụ trong bàng quang trong quá trình co bóp hoặc chèn ép bàng quang.
Giải phẫu sinh lý bàng quang hệ tiết niệu
Mặc dù phản xạ tiểu tiện là một phản xạ tủy sống tự chủ, nó cũng có thể bị ức chế hoặc tạo điều kiện cho các trung tâm ở vỏ não hoặc thân não.
Nephron: đơn vị chức năng của thận
Mỗi nephron chứa một chùm mao mạch cầu thận được gọi là cầu thận, qua đó một lượng lớn dịch được lọc từ máu, và một ống dài trong đó dịch đã lọc được chuyển hóa thành nước tiểu.
Cung cấp lưu lượng máu đến thận
Tuần hoàn thận là duy nhất ở chỗ có hai giường mao mạch, mao mạch cầu thận và màng bụng, được sắp xếp thành dãy và ngăn cách nhau bởi các tiểu động mạch.
Giải phẫu sinh lý của thận và hệ tiết niệu
Mặt giữa của mỗi quả thận chứa một vùng rốn, qua đó đi qua động mạch thận và tĩnh mạch, bạch huyết, cung cấp thần kinh và niệu quản, nơi mang nước tiểu cuối cùng từ thận đến bàng quang.
Những chức năng của thận
Thận thực hiện các chức năng quan trọng nhất của chúng bằng cách lọc huyết tương và loại bỏ các chất từ dịch lọc với tốc độ thay đổi, tùy thuộc vào nhu cầu của cơ thể.
Dịch trong khoảng trống tiềm ẩn của cơ thể
Hầu như tất cả các không gian tiềm ẩn đều có các bề mặt gần như tiếp xúc với nhau, chỉ có một lớp chất dịch mỏng ở giữa và các bề mặt trượt lên nhau.
Các yếu tố ngăn ngừa tình trạng phù
Khi áp lực gian bào lớn hơn 0 thì chỉ cần một sự thay đổi nhỏ áp lực cũng sẽ gây nên sự thay đổi thể tích lớn.
Các nguyên nhân gây phù ngoại bào
Có rất nhiều nguyên nhân gây phù ngoại bào, có thể chia làm 2 nhóm là tăng lọc qua mao mạch hay cản trở sự lưu thông hệ bạch huyết.
Phù: dịch dư thừa trong mô tế bào
Phù là tình trạng thừa dịch trong mô cơ thể. Nó thường liên quan đến dịch ngoại bào nhưng cũng co thể liên quan tới dịch nội bào.
Bất thường lâm sàng của điều chỉnh thể tích dịch: hạ và tăng natri máu
Hạ Na còn có thể do cơ thể hấp thu quá nhiều nước do tiết quá nhiều ADH, một hoocmon chống bài niệu, gây tái hấp thu quá nhiều nước vào cơ thể.
Glucose và dung dịch khác cho mục đích dinh dưỡng
Nhiều loại dịch được dùng qua đường tĩnh mạch để cung cấp chất dinh dưỡng cho cơ thể, trpng đó phổ biến nhất là glucose, ngoài ra còn có acid amin, lipid.
Cân bằng thẩm thấu được duy trì giữa dịch nội và ngoại bào
Nếu dung dịch muối đẳng trương được đưa vào ngoại bào thì nồng độ thẩm thấu sẽ không đổi, chỉ có thể tích dịch ngoại bào tăng lên.
Điều chỉnh trao đổi dịch và cân bằng thẩm thấu dịch trong và ngoài tế bào
Sự trao đổi giữa dịch nội bào và ngoại bào chủ yếu dựa vào chênh lêch áp suất thẩm thấu của những chất tan như Na, K, Cl.
Ngừng tuần hoàn trong shock: thời gian tổn thương não phụ thuộc vào tắc mạch
Trong nhiều năm, người ta đã dạy rằng tác động có hại này lên não là do tình trạng thiếu oxy não cấp tính xảy ra trong quá trình ngừng tuần hoàn.
Một số chỉ định điều trị shock
Bởi vì tác động có hại chính của hầu hết các loại shock là phân phối quá ít oxy đến các mô, việc cho bệnh nhân thở oxy có thể có lợi trong một số trường hợp.
Điều trị shock phản vệ và shock thần kinh: tác dụng của thuốc cường giao cảm
Thuốc cường giao cảm có tác dụng co mạch đối lập với tác dụng giãn mạch của histamine. Do đó, epinephrine, norepinephrine, hoặc các loại thuốc cường giao cảm khác thường là cứu cánh.
Điều trị shock: thay thế thể tích tuần hoàn trị liệu
Máu toàn phần không phải lúc nào cũng có sẵn, chẳng hạn như trong điều kiện chiến trường. Huyết tương thường có thể thay thế đầy đủ cho máu toàn phần vì nó làm tăng thể tích máu và phục hồi huyết động bình thường.
Shock nhiễm trùng: do vi khuẩn gram dương hoặc âm
Shock nhiễm trùng cực kỳ quan trọng đối với bác sĩ lâm sàng vì ngoài shock tim, shock nhiễm trùng là nguyên nhân thường xuyên nhất gây tử vong do shock.
Shock phản vệ và shock histamin
Shock phản vệ và shock histamin làm giảm đáng kể sự trở lại của tĩnh mạch và đôi khi shock nghiêm trọng đến mức bệnh nhân có thể chết trong vài phút.
Shock thần kinh: dung tích lòng mạch tăng lên
Một trong những nguyên nhân chính của shock thần kinh là đột ngột mất trương lực vận mạch khắp cơ thể, đặc biệt là làm giãn nở lớn các tĩnh mạch.
Shock giảm khối lương tuần hoàn do chấn thương
Nhiều nỗ lực đã được thực hiện để chỉ ra các yếu tố độc hại do các mô bị chấn thương tiết ra là một trong những nguyên nhân gây shock sau chấn thương.
Shock giảm khối lượng tuần hoàn do mất huyết tương
Shock giảm thể tích do mất huyết tương có các đặc điểm gần giống với shock do xuất huyết, ngoại trừ một yếu tố phức tạp khác.
Shock giảm khối lượng tuần hoàn không phục hồi
Trong tình trạng shock nặng, cuối cùng sẽ đạt đến giai đoạn mà bệnh nhân đó sẽ chết mặc dù liệu pháp điều trị tích cực vẫn có thể đưa cung lượng tim trở lại bình thường trong thời gian ngắn.
Shock: tiến triển và thoái triển của shock giảm khối lượng tuần hoàn
Nếu shock không đủ nghiêm trọng để chính nó gây ra sự tiến triển, cuối cùng sẽ hồi phục, nghĩa là các phản xạ giao cảm và các yếu tố khác đã bù đủ để ngăn chặn tuần hoàn suy giảm thêm.
Shock do giảm thể tích máu: shock mất máu
Giá trị đặc biệt của việc duy trì áp lực động mạch bình thường ngay cả khi giảm cung lượng tim là bảo vệ lưu lượng máu qua mạch vành và tuần hoàn não.
Sinh lý bệnh của shock tim
Shock thường do cung lượng tim không đủ. Do đó, bất kỳ tình trạng nào làm giảm cung lượng tim dưới mức bình thường đều có thể dẫn đến shock tim.
Phì đại tim: xẩy ra ở bệnh van tim và tim bẩm sinh
Phì đại tim thường được coi là phản ứng bù trừ của tim đối với khối lượng công việc tăng lên và thường có lợi cho việc duy trì cung lượng tim khi đối mặt với những bất thường làm giảm hiệu quả hoạt động của tim.
Tuần hoàn ngoài cơ thể: sử dụng trong phẫu thuật tim
Các hệ thống khác nhau đều gặp rất nhiều khó khăn, bao gồm tan máu, phát triển các cục máu đông nhỏ trong máu, khả năng các bong bóng oxy nhỏ hoặc các khối đệm nhỏ của chất chống tạo bọt đi vào động mạch.
Tứ chứng fallot: bệnh tim bẩm sinh shunt phải trái
Hầu hết máu giảm đi qua phổi, do đó máu động mạch chủ chủ yếu là máu tĩnh mạch chưa được oxy hóa. Trong tình trạng này, bốn bất thường của tim xảy ra đồng thời.
Tồn tại ống động mạch: bệnh tim bẩm sinh shunt trái phải
Ngay sau khi trẻ được sinh ra và bắt đầu thở, phổi sẽ phồng lên, các phế nang chứa đầy không khí mà sức cản của dòng máu qua cây mạch phổi cũng giảm rất nhiều, tạo điều kiện cho áp lực động mạch phổi giảm xuống.
Bệnh tim bẩm sinh: huyết động học bất thường thường gặp
Ảnh hưởng của các tổn thương tim khác nhau có thể dễ dàng hiểu được. Ví dụ, hẹp van động mạch chủ bẩm sinh gây ra các tác động tương tự như hẹp van động mạch chủ do các tổn thương van tim khác gây ra.
Bệnh van tim: huyết động học trong quá trình gắng sức thể lực
Ngay cả trong các trường hợp bệnh van tim nhẹ đến trung bình, dự trữ tim của bệnh nhân giảm tương ứng với mức độ nghiêm trọng của rối loạn chức năng van tim.
Bệnh van hai lá: huyết động học trong hẹp và hở van
Khi áp lực tâm nhĩ trái tăng lên, máu bắt đầu dồn lên phổi, cuối cùng trở lại động mạch phổi. Ngoài ra, phù nề phổi ngay từ đầu gây co thắt tiểu động mạch phổi.
Bệnh van động mạch chủ: ảnh hưởng của huyết động học trong hẹp và hở van
Lượng bù trừ quan trọng được diễn ra có thể cải thiện mức độ nghiêm trọng của các khuyết tật tuần hoàn. Một số cơ chế bù trừ được miêu tả.
Tiếng thổi của tim: được tạo ra bởi tổn thương của van
Các đồ thị chỉ ra cường độ của tiếng thổi thay đổi như thế nào trong suốt các phần khác nhau của thì tâm trương và thì tâm thu. Thời gian tương đối của mỗi tiếng thổi cũng là hiển nhiên.
Tổn thương van tim: tổn thương mắc phải và bẩm sinh
Van hai lá chịu nhiều chấn thương hơn so với các van khác, nó thương xuyên bị hư hỏng nghiêm trọng, và thứ hai là van đông mạch chủ thường xuyên bị tổn thương.
Phân tích biểu đồ suy tim cung lượng cao
Nếu tập thể dục, sẽ có dự trữ tim ít do khả năng của tim đã đạt được mức gần cực đại để bơm thêm lượng máu qua lỗ thông động tĩnh mạch. Tình trạng này được gọi là suy tim cung lượng cao.
Phân tích biểu đồ suy tim mất bù
Điều trị bệnh tim mất bù cho thấy tác dụng của digitalis trong việc nâng cao cung lượng tim, do đó làm tăng lượng nước tiểu và dịch chuyển dần dần của đường hồi lưu tĩnh mạch sang trái.
Dự trữ tim: đánh giả khả năng của tim khi nghỉ và khi gắng sức
Giảm dự trữ tim có thể do bệnh thiếu máu cơ tim, bệnh cơ tim nguyên phát, thiếu vitamin có thể ảnh hưởng đến cơ tim, tổn thương cơ tim, bệnh van tim, và nhiều yếu tố khác.
Suy tim: ứ dịch do thận gây phù ngoại vi
Giảm cung lượng tim thường làm giảm áp lực cầu thận do giảm huyết áp động mạch và co tiểu động mạch đến do cường giao cảm.
Phù ở bệnh nhân suy tim
Suy tim cấp nghiêm trọng thường gây giảm huyết áp mao mạch ngoại vi. Do đó, thử nghiệm trên động vật, cũng như thử nghiệm ở người, cho thấy suy tim cấp hầu hết không gây phù ngoại vi ngay lập tức.
Sốc do tim: suy tim giảm cung lượng tim
Hội chứng sốc tuần hoàn do tim bơm không đủ máu được gọi là sốc do tim. Một khi sốc do tim tiến triển, tỉ lệ sống sót thường nhỏ hơn 30% ngay cả khi có cấp cứu nhanh chóng.
Suy tim trái: nghẽn mạch phổi và phù phổi
Khi tim trái suy mà tim phải bình thường, máu tiếp tục được tống lên phổi nhờ tim phải, trong khi nó không được bơm ra khỏi phổi nhờ tim trái vào tuần hoàn hệ thống.
Suy tim mất bù: những thay đổi huyết động học trong suy tim nặng
Khi phát hiện tình trạng mất bù nghiêm trọng bằng tăng phù, đặc biệt là phù phổi, dẫn đến ran nổ và khó thở. Thiếu điều trị phù hợp trong giai đoạn cấp này có thể dẫn đến tử vong.
Suy tim cấp: những thay đổi huyết động học
Nhiều người đặc biệt là người già có cung lượng tim khi nghỉ ngơi bình thường nhưng có tăng nhẹ áp lực nhĩ phải do mức độ bù của suy tim.
Giai đoạn mạn của suy tim: sự giữ dịch và cung lượng tim được bù
Ảnh hưởng bất lợi của ứ quá nhiều dịch lên suy tim nặng. Ngược với ảnh hưởng tích cực của giữ dịch mức độ trung bình trong suy tim, quá nhiều dịch ứ đọng sẽ gây nên những hậu quả sinh lý nghiêm trọng.
Ảnh hưởng cấp tính của suy tim mức độ trung bình
Khi cung lượng tim giảm tạm thời, nhiều phản xạ tuần hoàn nhanh chóng được kích hoạt. Phản xạ được biết đến nhiều nhất là phản xạ thụ thể áp lực, được kích hoạt khi áp lực tâm nhĩ thay đổi.
Tuổi già và bệnh tật
Các bệnh này hoặc mới mắc hoặc mắc từ trẻ nay nặng lên. Trên thực tế, số người chết thuần tuý do già là rất hiếm.
Thay đổi trong quá trình lão hoá
Tuyến ức liên tục giảm kích thước và chức năng ngay từ khi cơ thể còn trẻ, đến tuổi trung niên thì thoái hoá hẳn
Các thuyết giải thích sự lão hoá
Tích luỹ các phân tử LDL bị oxy hoá bởi các gốc tự do, bị thu hút bởi các đại thực bào, tạo nên các tế bào bọt (foam cell) dẫn đến xơ vữa động mạch.
Những kết quả cơ bản nghiên cứu lão học
Chỉ số thời gian tỷ lệ chết tăng gấp đôi, mortality rate doubling time MRDT, Ở người MRDT là 8, nghĩa là cứ sau 8 năm, tỷ lệ chết lại tăng gấp đôi.
Đại cương sinh lý bệnh lão hóa
Tăng nhạy cảm với bệnh tật, tăng nguy cơ tử vong: hầu hết cơ thể già mang một hoặc nhiều bệnh và có tỷ lệ tử vong cao nhất so với mọi giai đoạn phát triển trước đó.
Sinh lý bệnh ung thư
Tác dụng gián tiếp qua chuyển hoá (tiền thân chất gây ung thư): sau khi đưa vào cơ thể thì sẽ được các enzym hay vi khuẩn đường ruột biến đổi trở thành chất gây ung thư.
Chu kỳ tế bào và cơ chế sửa sai trong sao chép
Bộ gen tuyến trùng Caenorhabditis elegans có 1031 gen, trong đó có 131 gen có phân định sẳn là chết theo chương trình.
Đại cương rối loạn phát triển tổ chức
Mọi sinh vật đều được cấu tạo từ các tế bào, các tế bào họp thành các mô, các mô họp thành các cơ quan như tim, phổi, gan.v.v.
Ý nghĩa sinh học của viêm
Phản ứng viêm nói chung là phương tiện để bảo vệ cơ thể khi yếu tố có hại xuất hiện, tuy nhiên khi phản ứng viêm xảy ra quá mức cũng gây nhiều biến loạn cho cơ thể.
Mối liên quan giữa ổ viêm và toàn thân
Ngày nay, người ta biết dùng corticoid và các thuốc kháng viêm không steroid, để làm giảm bớt hiện tượng viêm khi cần thiết
Sinh lý bệnh viêm mạn
Viêm mạn theo sau viêm cấp do đáp ứng viêm không thành công, ví dụ còn tồn tại VK hay dị vật trong vết thương làm cho phản ứng viêm kéo dài.
Sinh lý bệnh viêm cấp
Các tế bào và tiểu cầu thực hiện các chức năng với sự hỗ trợ của 3 hệ thống protein huyết tương đó là hệ thống bổ thể, hệ thống đông máu, hệ thống kinin.
Đại cương về viêm
Virchow (thế kỷ XIX) đã cho rằng viêm là phản ứng cục bộ, nhưng hiện tại người ta cho rằng viêm là biểu hiện cục bộ của một phản ứng toàn thân.
Sinh lý bệnh về sốt
Ngày nay người ta biết, có nhiều chất có tác động lên trung tâm điều nhiệt, gây sốt được sản xuất từ nhiều loại tế bào khác nhau, gọi chung là các cytokine gây sốt.
Rối loạn thân nhiệt
Giảm thân nhiệt bệnh lý có thể xảy ra trong các trường hợp bệnh lý có rối loạn chuyển hóa trầm trọng như: xơ gan, tiểu đường, suy dinh dưỡng, shock
Đại cương về điều hoà thân nhiệt
Bình thường có sự cân bằng giữa hai quá trình sinh nhiệt và thải nhiệt, để giữ cân bằng phải có sự tham gia của hệ thần kinh trung ương, đó là trung tâm điều nhiệt.
Các chỉ số cơ bản trong rối loạn cân bằng Acid Base
Các chỉ số cần theo dõi.(Giá trị bình thường) pH = 7,36 - 7,45. PaCO2 = 35 - 45 mmHg. HCO3- = 22 - 27 mmol/l. BE = (-1) đến (+2) mmol/l.
Cơ chế bù trừ trong nhiễm Acid Base
Sự di chuyển của Cl- từ huyết tương vào trong hồng cầu và HCO3- từ hồng cầu ra huyết tương do CO2 tăng lên ở tổ chức (hiện tượng Hamberger).
Cân bằng Acid Base và cân bằng Kali
Trường hợp nhiễm kiềm chuyển hóa: H+ đi ra khỏi tế bào, K+ đi vào tế bào. Do đó nhiễm kiềm chuyển hóa sẽ đưa đến hạ kali máu.
Bài giảng rối loạn cân bằng Acid Base
Nhiễm độc acid, hay nhiễm toan, là một quá trình bệnh lý, có khả năng làm giảm pH máu xuống dưới mức bình thường.
Đại cương rối loạn cân bằng acid base
Hầu hết các phản ứng chuyển hóa xảy ra trong cơ thể luôn đòi hỏi một pH thích hơp, trong khi đó phần lớn các sản phẩm chuyển hóa của nó.
Bài giảng rối loạn cân bằng nước điện giải
Sự tiết ADH vẫn xãy ra ngay cả khi đáng lẽ ra nó phải được ức chế. Sự tăng tiết ADH này có nguồn gốc thể tạng đưa đến sự bài tiết nước tự do qua thận bị thay đổi trong khi sự điều hòa cân bằng muối là bình thường.
Đại cương sinh lý bệnh cân bằng nước điện giải
Kích thích chủ yếu của sự nhập nước là khát, xuất hiện khi áp lực thẩm thấu hiệu quả tăng hoặc thể tích ngoại bào hay huyết áp giảm.
Bài giảng rối loạn chuyển hóa protid
Giảm protid huyết tương phản ánh tình trạng giảm khối lượng protid của cơ thể, một gam protid huyết tương đại diện cho 30 gam protid của cơ thể.
Sinh lý và hóa sinh chuyển hóa protid
Protid mang mã thông tin di truyền và là bản chất của nhiều hoạt chất sinh học quan trọng như enzym, kháng thể, bổ thể, hormon peptid
Sinh lý bệnh gan nhiễm mỡ
Nhìn chung biểu hiện lâm sàng thường kín đáo và tiến triển thường nhẹ, vì mỡ không phải là chất độc, nó chỉ gây ra tác động cơ học là gan hơi lớn.
Sinh lý bệnh rối loạn chuyển hóa lipid
Tùy theo phương pháp, có thể đánh giá khối lượng mỡ toàn phần, hoặc sự phân bố mỡ trong cơ thể.
Sinh lý và hóa sinh lipid
Lipid tham gia cấu trúc cơ thể và là bản chất của một số hoạt chất sinh học quan trọng như: phospholipid tham gia cấu trúc màng tế bào và là tiền chất của prostaglandin và leucotrien.
Rối loạn cân bằng glucose máu
Trong đói dài ngày, giảm glucose máu có biểu hiện lâm sàng trung bình sau khoảng 50 ngày (đối với người khỏe mạnh) do kiệt cơ chất cần cho sinh đường mới.
Nhắc lại sinh lý sinh hóa glucose máu
Tất cả các loại glucid đều được chuyển thành đường đơn trong ống tiêu hóa và được hấp thu theo thứ tự ưu tiên như sau: galactose, glucose, fructose và pentose.
Sinh lý bệnh tử vong
Hoạt động của tim và phổi ngừng hẳn, lúc nầy thần kinh trung ương hoàn toàn bị ức chế do không còn quá trình oxy hóa vì rối loạn enzyme hô hấp.
Quá trình bệnh lý
Thời kỳ tiệm phát có thể kéo dài mấy ngày và nếu sức đề kháng của cở thể mạnh thì bệnh cũng có thể kết thúc trong giai đoạn nầy, ta gọi là bệnh ở thể sẩy.
Một số vấn đề quan trọng trong bệnh sinh học
Cục bộ và toàn thân: một tổn thương tại chỗ, gây nên bất cứ do yếu tố bệnh nguyên nào, xét cho cùng cũng sẽ ảnh hưởng đến toàn thân.
Định nghĩa bệnh sinh
Trong điều trị học, nếu biết được nguyên nhân để điều trị là tốt nhất nhưng nếu không biết được nguyên nhân thì điều trị theo cơ chế bệnh sinh.
Phân loại bệnh nguyên
Ô nhiễm tiếng ồn không chỉ ảnh hưởng đến thính lực mà còn là nguy cơ dẫn đến các chứng bệnh như huyết áp cao, bệnh tim mạch
Quan niệm khoa học về bệnh nguyên
Nguyên nhân quyết định tính đặc hiệu của bệnh. Nguyên nhân và những điều kiện nhất định gây nên một bệnh gọi chung là các yếu tố bệnh nguyên.
Một số quan niệm chưa đầy đủ về bệnh nguyên
Do không phân biệt được nguyên nhân và điều kiện hoặc không phân biệt được vai trò của mỗi yếu tố trong quá trình gây bệnh
Định nghĩa bệnh nguyên
Về lý luận, nó thể hiện rõ lập trường duy tâm hay duy vật. Về thực hành, nó quyết định kết quả của công tác phòng bệnh và điều trị bệnh.
Một số điểm cần chú ý để hiểu khái niệm bệnh
Khi cơ thể bị bệnh vẫn có một sự cân bằng, đó là cân bằng bệnh lý: Yếu tố gây bệnh ( hủy hoại bệnh lý = Phản ứng cơ thể ( phòng ngự sinh lý.
Sơ lược sự phát triển về khái niệm bệnh
Bệnh là do rối loạn các thể dịch đó. Ví dụ: có quá nhiều dịch nhầy ở khắp nơi như ở phổi , ở ổ bụng, ở ruột, ở trực tràng
Phương pháp nghiên cứu trong sinh lý bệnh
Các thực nghiệm khoa học thường xây dựng các mô hình thực nghiệm trên súc vật từ những quan sát lâm sàng để chứng minh cho các giả thuyết đề ra.
Vị trí tính chất và vai trò của môn sinh lý bệnh
Môn sinh lý bệnh, như định nghĩa đã nêu rõ; đi từ những hiện tượng bệnh lý cụ thể, tìm cách khái quát hóa thành những quy luật.
Sinh lý bệnh soi sáng công tác dự phòng và điều trị
Sự hiểu biết về vai trò của nguyên nhân và điều kiện gây bệnh sẽ giúp cho việc đề ra kế hoạch phòng bệnh đúng.
Đại cương sinh lý bệnh
Tất cả xuất phát từ hiện tượng đi tìm bản chất của vấn đề là tìm hiểu được bệnh là gì ? bệnh do đâu mà có ? bệnh tiến triển như thế nào? quá trình lành bệnh và tử vong xảy ra như thế nào?.