- Trang chủ
- Sách y học
- Bài giảng sinh lý bệnh
- Hồng cầu: sản sinh biệt hóa và tổng hợp
Hồng cầu: sản sinh biệt hóa và tổng hợp
Hầu hết hồng cầu được sản xuất tại các xương có màng như xương cột sống, xương ức, các xương sườn và các xương chậu. Thậm chí, các xương này cũng giảm sản xuất khi tuổi tăng lên.
Biên tập viên: Trần Tiến Phong
Đánh giá: Trần Trà My, Trần Phương Phương
Nơi sản xuất tế bào hồng cầu trong cơ thể
Trong những tuần đầu của phát triển phôi thai, nguyên thủy, hồng cầu có nhân được sản xuất trong túi noãn hoàng. Ở 3 tháng giữa thai kỳ, gan là cơ quan chính sản xuất hồng cầu, nhưng một số lượng vừa phải hồng cầu cũng được sản xuất tại lách và các hạch lympho. Sau đó, trong khoảng tương đương tháng cuối thai kỳ và sau khi sinh, hồng cầu chỉ duy nhất được sản xuất tại tủy xương.
Ở hình, tủy xương của các xương chủ yếu sản xuất hồng cầu đến khi 5 tuổi. Tủy của các xương dài, ngoại trừ đầu gần của xương cánh tay và xương chày, trở nên tích mỡ và không sản xuất hồng cầu sau 20 tuổi. Qua tuổi này, hầu hết hồng cầu được sản xuất tại các xương có màng như xương cột sống, xương ức, các xương sườn và các xương chậu. Thậm chí, các xương này cũng giảm sản xuất khi tuổi tăng lên.
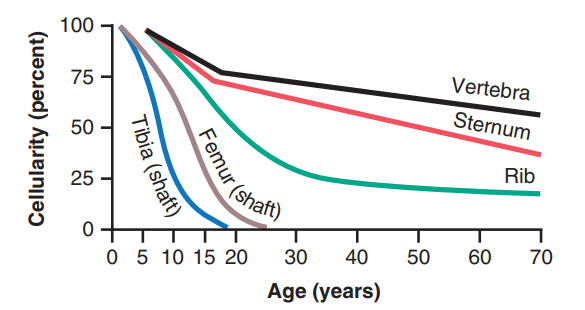
Hình. Tỷ lệ sản xuất hồng cầu tương đối trong tủy xương của các xương khác nhau ở các độ tuổi khác nhau.
Bắt đầu tổng hợp các tế bào máu
Các tế bào gốc sinh máu vạn năng, các kích tố tăng trưởng và các kích tố biệt hóa. Các tế bào máu bắt nguồn từ tủy xương từ một dạng tế bào đơn giản gọi là Tế bào gốc sinh máu vạn năng, đó là nơi bắt nguồn của tất cả các tế bào của máu tuần hoàn. Hình cho thấy sự phân chia kế tiếp liên tục của các tế bào vạn năng tạo thành các tế bào khác nhau của hệ tuần hoàn. Khi các tế bào này sinh sản, có một tỷ lệ nhỏ các tế bào vạn năng được giữ lại trong tủy xương để duy trì sự cung cấp các tế bào máu cho hệ tuần hoàn, mặc dù số này cũng giảm đi theo tuổi tác. Tuy nhiên, hầu hết các tế bào được sinh ra lại tiếp tục biệt hóa để tạo ra các loại tế bào còn lại về phía bên phải của hình Các tế bào ở giai đoạn trung gian rất giống với tế bào gốc vạn năng dù chúng đã hoàn toàn trở thành một dòng tế bào riêng biệt và được gọi là tế bào gốc (CSCs).
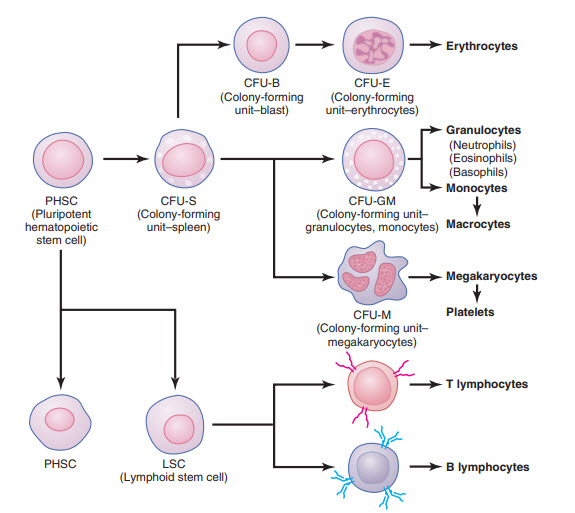
Hình. Hình thành nhiều tế bào máu khác nhau từ tế bào gốc tạo máu đa năng ban đầu trong tủy xương.
Các tế bào gốc khác nhau khi được nuôi cấy sẽ sản sinh ra các cụm riêng biệt của các tế bào máu. Một tế bào gốc sản sinh ra hồng cầu thì được gọi là đơn vị tạo cụm dòng hồng cầu (colony-forming unit-erythrocyte) viết tắt là CFU-E. Tương tự như vậy, Đơn vị tạo cụm dòng bạch cầu hạt và mono cũng được viết tắt là CFU-GM và cứ như thế cho các cụm khác.
Sự sinh trưởng và sinh sản của các tế bào gốc khác nhau được điều khiển bởi nhiều protein gọi là các kích tố tăng trưởng ( growth inducers). Có ít nhất 4 kích tố tăng trưởng chính đã được mô tả, mỗi kích tố có các đặc điểm khác nhau. Một trong số đó là interleukin-3, kích thích sự tăng trưởng và sinh sản của hầu hết tất cả các tế bào gốc khác nhau, trong khi các kích tố còn lại chỉ kích thích sự tăng trưởng của một vài loại tế bào.
Các kích tố tăng trưởng kích thích tăng trưởng nhưng không biệt hóa tế bào, mà là chức năng của một bộ protein khác gọi là các kích tố biệt hóa (differentiation inducers). Mỗi kích tố loại này chỉ gây biệt hóa một loại tế bào gốc biệt hóa một hay nhiều bước để trở thành tế bào máu trưởng thành cuối cùng.
Sự hình thành của các kích tố biệt hóa và tăng trưởng được điều khiển bởi các yếu tố bên ngoài tủy xương. Ví dụ, với các tế bào hồng cầu, sự thiếu oxygen trong máu trong một thời gian dài sẽ gây ra kích thích, biệt hóa và sản xuất một lượng lớn hồng cầu, sẽ được thảo luận phần sau chương này. Trong trường hợp một số tế bào bạch cầu, các bệnh nhiễm khuẩn gây ra tăng trưởng và biệt hóa, tạo thành một số loại cuối cùng của các tế bào bạch cầu cần cho chống lại từng tác nhân riêng.
Các giai đoạn biệt hóa của hồng cầu
Tê bào đầu tiên có thể xác định thuộc về dòng hồng cầu đó là tiền nguyên hồng cầu (proerythroblast), được trình bày ở điểm bắt đầu của hình. Dưới sự kích thích phù hợp, một lượng lớn các tế bào này được hình thành từ các tế bào CFU-E.
Khi được hình thành, Tiền nguyên hồng cầu tiếp tục phân chia nhiều lần, cuối cùng tạo ra nhiều tế bào hồng cầu trưởng thành. Thế hệ tế bào đầu tiên được gọi là các Nguyên hồng cầu ưa base (basophil erthyroblasts) vì chúng bắt màu thuốc nhuộm căn bản; lúc này tế bào đã tích lũy một lượng rất ít Hemoglobin. Ở thế hệ tiếp theo, như trong hình, các tế bào được lấp đầy bởi Hemoglobin đến 34%, nhân tế bào đông tụ nhỏ lại, phần còn sót lại cuối cùng bị hấp thụ hoặc loại bỏ từ tế bào đó. Cùng lúc đó, lưới nội chất cũng bị tái hấp thụ. Tế bào ở giai đoạn này được gọi là Hồng cầu lưới (reticulocyte) vì vẫn còn lại một lượng nhỏ chất ưa base, đó là phần sót lại của Bộ máy Golgi, ti thể và một ít các bào quan khác của tế bào chất. Trong giai đoạn Hồng cầu lưới này, các tế bào đi từ tủy xương ra mao mạch máu bằng Xuyên mạch (chui qua các khe của màng mao mạch).
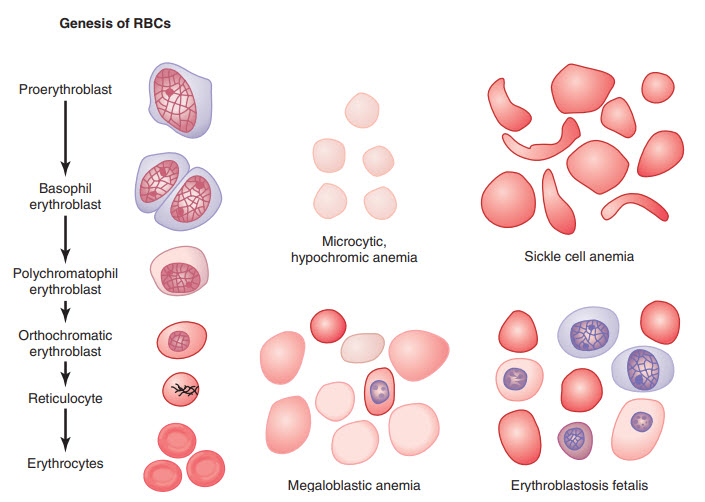
Hình. Nguồn gốc của tế bào hồng cầu bình thường (RBCs) và đặc điểm của tế bào hồng cầu trong các loại thiếu máu cục bộ.
Phần vật chất ưa base còn lại trong Hồng cầu lưới thường biến mất sau 1-2 ngày để thành Hồng cầu trưởng thành. Do đời sống ngắn nên Hồng cầu lưới chiếm dưới 1% trong tổng số hồng cầu trong máu.
Erythropoietin điều hòa sản sinh hồng cầu
Tổng khối lượng hồng cầu trong máu được điều chỉnh trong một giới hạn hẹp, và do đó (1) một lượng đủ hồng cầu luôn đảm bảo vận chuyển đủ oxygen từ hai phổi đến các mô, và (2) không trở nên quá nhiều có thể làm cản trở dòng máu. Cơ chế điều khiển này được sơ đồ hóa ở hình và được mô tả ở các phần sau.
Sự oxi hóa tại mô là yếu tố điều hòa thiết yếu nhất cho sự sản xuất hồng cầu. Trường hợp mà lượng oxygen được vận chuyển đến mô bị giảm đi thường làm tăng sản sinh hồng cầu. Do vậy, khi một người bị thiếu máu nhiều có thể do xuất huyết hoặc nguyên nhân khác, tủy xương sẽ sản sinh lượng lớn hồng cầu. Cũng vì thế, sự phá hủy phần lớn tủy xương, đặc biệt bởi tia X, gây nên sự quá sản của phần tủy xương còn lại để cung cấp đủ hồng cầu cho cơ thể.
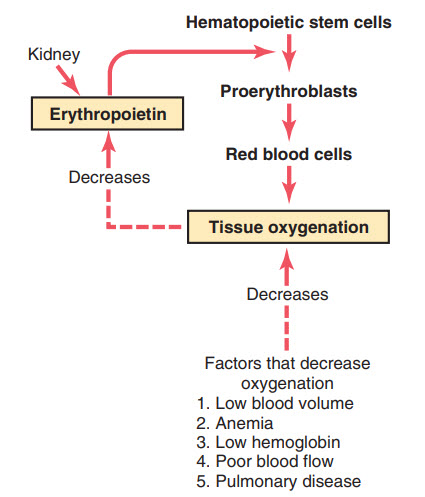
Hình. Chức năng của erythropoietin để tăng sản xuất hồng cầu khi oxy hóa mô giảm.
Ở độ cao lớn, lượng oxygen trong không khí bị giảm mạnh, lượng oxygen cung cấp cho mô không đủ sẽ làm tăng mạnh sự sản sinh hồng cầu. Trong trường hợp này, yếu tố điều khiển sự sản sinh hồng cầu không phải là nồng độ hồng cầu trong máu mà là nhu cầu oxygen của mô.
Nhiều bệnh của hệ tuần hoàn làm giảm dòng máu trong mô, đặc biệt những bệnh gây ra sự giảm hấp thu oxygen bởi dòng máu khi đi qua phổi, có thể tăng mức sản sinh hồng cầu. Điều này khá điển hình trong bệnh suy tim và nhiều bệnh phổi vì sự thiếu oxi mô từ những bệnh này làm tăng sản sinh hồng cầu, và do đó làm tăng hematocrit cũng như tổng thể tích máu.
Erythropoietin kích thích sản sinh hồng cầu và chúng tăng khi thiếu oxygen
Kích thích chủ yếu để sinh sản hồng cầu khi thiếu oxi là một hoormon tuần hoàn tên là erythropoietin, một glycoprotein có trọng lượng phân tử khoảng 34000. Khi thiếu erythropoietin, thiếu oxi sẽ ít hoặc không kích thích được sinh sản hồng cầu. Tuy nhiên, khi hệ erythropoietin bình thường, sự thiếu oxi sẽ làm tăng đáng kể sản xuất erythropoietin, do đó làm tăng sản hồng cầu đến khi nhu cầu oxi được thỏa mãn.
Erythropoietin được sinh ra chủ yếu ở thận. Bình thường, khoảng 90% erythropoietin được sản xuất tại thận, phần còn lại chủ yếu tại gan. Chưa rõ chính xác nó được sản xuất ở đâu trong thận. Vài nghiên cứu cho rằng erythropoietin được sản xuất bởi tế bào giống nguyên bào sợi gian bào bao quanh các ống tại vùng vỏ và tủy ngoài, nơi có nhu cầu oxi cao. Và có lẽ các tế bào khác, gồm cả các tế bào biểu mô thận cũng tiết erythropoietin để đáp ứng với thiếu oxi.
Thiếu máu mô thận dẫn đến tăng mức Yếu tố cảm ứng thiếu oxi (HIF-1: hypoxia-inducible factor-1) trong mô, giống như một yếu tố phiên mã cho số lượng lớn các gen cảm ứng thiếu oxi, trong đó có gen erythropoietin. HIF-1 gắn với phần tử đáp ứng thiếu oxi trên gen erythropoietin, gồm có tổng hợp mRNA và cuối cùng tăng tổng hợp erythropoietin.
Đôi khi, thiếu máu không tại thận kích thích thận tiết erythropoietin, điều đó cho thấy, có thụ cảm ngoài thận gửi tín hiệu về thận để sản xuất hoormon này. Đặc biệt, cả norepinephrine và epinephrine và nhiều prostaglandin khác cũng kích thích tổng hợp erythropoietin.
Khi cắt bỏ cả 2 thận hoặc chúng bị hư hại bởi các bệnh tại thận thì người đó sẽ trở nên thiếu máu nặng do 10% erythropoietin còn lại được sản xuất tại các mô khác (chủ yếu tại gan) chỉ đáp ứng được 1/3 đến 1/2 sự tổng hợp oxi mà cơ thể cần.
Erythropoietin kích thích sản xuất Tiền nguyên hồng cầu từ Tế bào gốc sinh máu vạn nặng. Khi ở trong môi trường thiếu oxi, erythropoietin sẽ được sản xuất trong vòng vài phút đến vài giờ và đạt đỉnh sau 24h. Tuy nhiên vẫn chưa có tế bào hồng cầu mới nào xuất hiện trong máu trong vòng 5 ngày sau đó. Từ đó, cũng từ những nghiên cứu khác, người ta khẳng định rằng, tác động quan trọng của erythropoietin là kích thích sản xuất Tiền nguyên hồng cầu từ Tế bào gốc sinh máu vạn năng trong tủy xương. Thêm vào đó, sau khi tạo ra nhiều Tiền nguyên hồng cầu, nó lại đẩy nhanh các giai đoạn nguyên hồng cầu sau đó và nhanh tạo hồng cầu. Việc sản xuất nhanh này sẽ tiếp tục diễn ra khi còn trong trạng thái thiếu oxi hoặc cho đến khi sản xuất đủ lượng hồng cầu để mang đủ lượng oxi đến mô dù mức oxi không khí thấp; lúc này, mức tổng hợp erythropoietin sẽ giảm đến mức duy trì tổng hợp đủ hồng cầu cho máu mà không thừa.
Nếu thiếu erythropoietin, có ít hồng cầu được tổng hợp bởi tủy xương. Ở một thái cực khác, nếu sản xuất nhiều erythropoietin, có đủ sắt và các chất dinh dưỡng khác thì mức sản xuất hồng cầu có thể tăng gấp 10 lần hoặc hơn so với bình thường. Do vậy, erythropoietin là một cơ chế điều khiển mạnh mẽ quá trình tổng hợp hồng cầu.
Sự trưởng thành của hồng cầu cần vitamin B12 (Cyanocobalamin) và Acid Folic
Do sự cần tiếp tục lấp đầy hồng cầu, các tế bào dòng hồng cầu là các tế bào sinh sản và sinh trưởng nhanh nhất của cơ thể. Do đó, sự trưởng thành và mức sinh sản của chúng phụ thuộc nhiều vào chế độ dinh dưỡng của cơ thể.
Đặc biệt quan trọng cho sự trưởng thành cuối cùng của hồng cầu là 2 vitamins, vitamin B12 và acid folic. Cả 2 đều thiết yếu cho sự tổng hợp DNA, vì mỗi vitamin theo cách khác nhau, cần thiết cho sự tổng hợp của thymidine triphosphate, một trong các đơn vị cơ bản cấu tạo DNA. Vì vậy, thiếu vitamin B12 cũng như acid folic sẽ tạo ra DNA bất thường hoặc thiếu, và dẫn đến sai sót trong trưởng thành của nhân và phân chia tế bào. Thêm vào đó, các nguyên hồng cầu không những không tăng sinh nhanh chóng được mà còn sinh ra các tế bào lớn hơn hồng cầu bình thường và gọi là Tế bào khổng lồ ( macrocytes), tế bào loại này có màng không bền thường có hình oval lớn không cân đối thay vì hình đĩa lõm 2 mặt như thường. Những tế bào này, khi vào tuần hoàn chung vẫn có khả năng mang oxi nhưng có đời sống ngắn do dễ vỡ, bằng 1/2 đến 1/3 bình thường. Vậy, thiếu vitamin B12 cũng như acid folic gây nên Sự trưởng thành thất bại (maturation failure) trong quá trình tổng hợp hồng cầu.
Maturation Failure (MF) gây ra do thiếu hấp thu vitamin B12 trong ống tiêu hóa-Thiếu máu ác tính. Nguyên nhân thường gặp gây thiếu máu ác tính là do giảm hấp thu vitamin B12 trong ống tiêu hóa, thường do teo niêm mạc dạ dày làm giảm tiết dịch vị. Tế bào thành của dạ dày sản xuất ra một glycoprotein gọi là yếu tố nội, gắn với vitamin B12 trong thức ăn và ruột có thể hấp thu. Cơ chế như sau:
Yếu tố nội gắn chặt với vitamin B12. Bảo vệ cho vitamin không bị tiêu hóa bởi dịch vị.
Trong khi gắn, yếu tố nội gắn với receptor đặc hiệu trên màng tế bào diềm bàn chải của niêm mạc hồi tràng.
Vitamin B12 được đưa vào máu trong vài giờ sau đó bởi sự ẩm bào cả yếu tố nội và vitamin qua màng.
Thiếu yếu tố nội làm giảm vitamin B12 do giảm hấp thu. Khi vitamin B12 được hấp thu vào máu, đầu tiên nó sẽ được dự trữ lượng lớn tại gan và giải phóng chậm theo nhu cầu của tủy xương. Lượng vitamin B12 nhỏ nhất cần để duy trì sự trưởng thành bình thường của hồng cầu mỗi ngày khoảng 1-3 micrograms, và lượng dự trữ tại gan và các mô khác gấp khoảng 1000 lần lượng này. Do đó, giảm hấp thu vitamin B12 trong 3-4 năm thường mới gây thiếu máu do MF.
MF do thiếu acid folic (acid pteroylglutamic). Acid Folic thông thường có ở nhiều loại rau xanh, trái cây, và thịt ( đặc biệt trong gan ). Tuy nhiên nó dễ bị phá hủy khi đun nấu. Cũng như thế, người bị bệnh rối loạn hấp thu, ví như bệnh ruột non thường xuát hiện gọi là sprue ( tiêu chảy nhiệt đới), thường gây cản trở hấp thu nghiêm trọng cả vitamin B12 và acid folic. Do vậy, trong nhiều trường hợp thiếu máu MF, nguyên nhân là giảm hấp thu cả acid folic và vitamin B12 tại ruột.
Bài viết cùng chuyên mục
Nhắc lại sinh lý sinh hóa glucose máu
Tất cả các loại glucid đều được chuyển thành đường đơn trong ống tiêu hóa và được hấp thu theo thứ tự ưu tiên như sau: galactose, glucose, fructose và pentose.
Áp suất thẩm thấu và nồng độ natri của cơ thể
Sự gia tăng áp suất thẩm thấu dịch ngoại bào làm cho các tế bào thần kinh đặc biệt gọi là các tế bào osmoreceptor, nằm ở phần trước vùng dưới đồi gần các nhân opraotic, co rút lại.
Thận bài tiết nước dư thừa bằng cách hình thành nước tiểu loãng
Thận bình thường có một khả năng rất lớn để thay đổi tỷ lệ tương đối của các chất tan và nước trong nước tiểu để đáp ứng với những thách thức khác nhau.
Hội chứng Brown Sequard: liệt vận động cùng bên tổn thương
Hội chứng Brown - Séquard gây những hệ quả có thể dự đoán được nhờ vào kiến thức về chức năng các bó trong tủy sống. Theo đó, toàn bộ chức năng vận động đều bị ngăn chặn ở bên cùng phía với tổn thương.
Tật khúc xạ: cận thị và viễn thị
Một người thường chọn độ hội tụ của kính phân kì hay kính hội tụ cần thiết bằng “phương pháp thử” - đó là, đầu tiên, thử một kính có độ hội tụ bất kì sau đó tiếp tục thử kính khác.
Giải phẫu sinh lý bàng quang hệ tiết niệu
Mặc dù phản xạ tiểu tiện là một phản xạ tủy sống tự chủ, nó cũng có thể bị ức chế hoặc tạo điều kiện cho các trung tâm ở vỏ não hoặc thân não.
Chuyển hóa fibrinogen thành fibrin: hình thành cục máu đông
Cục máu đông là một mạng lưới sợi fibrin chạy theo mọi hướng và giam giữ các tế bào máu, tiểu cầu và huyết tương. Các sợi fibrin cũng gắn với bề mặt mạch máu bị tổn thương.
Sinh lý bệnh của say nóng
Trong số những thay đổi sinh lý quan trọng trong qua trình thích nghi với tăng nhiệt độ gồm tăng lượng mồ hôi tối đa gấp 2 lần, tăng thể tích huyết tương, và giảm lượng muối mất qua mồ hôi và nước tiểu.
Tái hấp thu ở ống thận: bao gồm các cơ chế thụ động và chủ động
Chất tan được vận chuyển qua tế bào bởi vận chuyển chủ động hoặc thụ động, hay giữa các tế bào bằng cách khuyếch tán. Nước được vận chuyển qua tế bào và giữa các tế bào ống thận bằng cách thẩm thấu.
Kiểm soát sự bài tiết canxi ở thận và nồng độ ion canxi ngoại bào
Đường tiêu hóa và các cơ chế điều hòa ảnh hưởng đến sự hấp thu và bài tiết canxi ở ruột đóng một vai trò quan trọng trong việc cân bằng canxi nội môi.
Sự hình thành bạch cầu: quá trình hình thành trong tủy xương
Bạch cầu được hình thành trong tủy xương được dự trữ trong tủy xương đến khi chúng cần thiết phải đi vào hệ tuần hoàn. Sau đó, khi có nhu cầu, các yếu tố khác nhau làm cho chúng được giải phóng.
Bộ đệm Protein: điều chỉnh thăng bằng kiềm toan nội bào
Ngoài nồng độ cao trong tế bào, một yếu tố khác góp phần vào khả năng đệm của protein là pKs của nhiều hệ thống protein khá gần với pH nội bào.
Một số điểm cần chú ý để hiểu khái niệm bệnh
Khi cơ thể bị bệnh vẫn có một sự cân bằng, đó là cân bằng bệnh lý: Yếu tố gây bệnh ( hủy hoại bệnh lý = Phản ứng cơ thể ( phòng ngự sinh lý.
Động lực học của mao mạch phổi: trao đổi dịch mao mạch và động lực học dịch kẽ phổi
Phù phổi xảy ra cùng cách phù nề xảy ra ở những nơi khác trong cơ thể. Bất kì yếu tố làm tăng lọc dịch lỏng ra khỏi mao mạch phổi hoặc cản trở chức năng bạch huyết phổi và gây ra tăng áp lực lọc phổi kẽ từ âm sang dương.
Miễn dịch và dị ứng: đề kháng của cơ thể trong nhiễm khuẩn
Miễn dịch bẩm sinh làm cho cơ thể con người đề kháng các bệnh như một số bệnh nhiễm virus bại liệt của động vật, bệnh tả heo, gia súc bệnh dịch, và bệnh distemper.
Cân bằng thẩm thấu được duy trì giữa dịch nội và ngoại bào
Nếu dung dịch muối đẳng trương được đưa vào ngoại bào thì nồng độ thẩm thấu sẽ không đổi, chỉ có thể tích dịch ngoại bào tăng lên.
Bài tiết H + chủ động: trong các tế bào kẽ của ống lượn xa và ống góp
Mặc dù sự bài tiết H+ ở đoạn cuối ống lượn xa và ống góp chỉ chiếm khoảng 5% của tổng H+ bài tiết. Nhưng cơ chế này rất quan trọng trong việc acid hóa tối đa nước tiểu.
Bạch cầu ưa base (bạch cầu ái kiểm): vai trò quan trọng trong phản ứng dị ứng
Dưỡng bào và bạch cầu ái kiềm đóng một vai trò quan trọng trong nhiều loại phản ứng dị ứng bởi lọai kháng thể gây ra phản ứng dị ứng, IgE có xu hướng đặc biệt gắn với dưỡng bào và bạch cầu ái kiềm.
Cơ chế bệnh sinh của xơ vữa động mạch
Các mảng xơ vữa bám vào còn ảnh hưởng tới dòng máu chảy, bề mặt thô ráp của chúng làm cho các cục máu đông phát triển tại đó, tạo thành huyết khối tại chỗ hoặc cục máu đông.
Tự điều hòa mức lọc cầu thận để ngăn ngừa thay đổi bài tiết của thận
Những cơ chế kiểm soát đặc biệt, thay đổi huyết áp vẫn có những ảnh hưởng đáng kể về bài tiết nước và muối; này được gọi là nhiều áp lực tiểu hoặc bài niệu natri áp lực, và nó là rất quan trọng trong việc điều tiết lượng dịch cơ thể và huyết áp.
Sinh lý bệnh của bệnh đần độn
Thiếu hụt bẩm sinh tuyến giáp, tuyến giáp không có khả năng sản xuất hormon giáp do khiếm khuyết một gen của tuyến, hoặc do thiếu hụt iod trong chế độ ăn.
Màng mao mạch cầu thận: bước đầu hình thành nước tiểu
Khả năng lọc của chất tan tỉ lệ ngịch với kích thước của chúng. Màng mao mạch cầu thận dày hơn các mao mạch khác, nhưng có nhiều lỗ nhỏ hơn và do đó lọc dịch tốc độ cao.
Hồng cầu máu: nồng độ hình dạng kích thước và chức năng
Các tế bào hồng cầu có chức năng khác ngoài vận chuyển hemoglobin, nó chứa một lượng lớn carbonyc anhydrase, một enzyme xúc tác cho phản ứng thuận ngịch giữa CO2 và nước tạo ra carbonic acid (H2CO3), làm tăng tốc độ phản ứng.
Hấp thụ và bài tiết natri: được cân bằng trong trạng thái ổn định
Nếu rối loạn chức năng thận không quá nghiêm trọng, có thể đạt được cân bằng natri chủ yếu bằng cách điều chỉnh nội thận với những thay đổi tối thiểu về thể tích dịch ngoại bào hoặc các điều chỉnh toàn thân khác.
Phù: dịch dư thừa trong mô tế bào
Phù là tình trạng thừa dịch trong mô cơ thể. Nó thường liên quan đến dịch ngoại bào nhưng cũng co thể liên quan tới dịch nội bào.
