- Trang chủ
- Sách y học
- Bài giảng sinh lý bệnh
- Cơ chế bệnh sinh của gầy mòn chán ăn và suy nhược
Cơ chế bệnh sinh của gầy mòn chán ăn và suy nhược
Kho dự trữ chất béo hoàn toàn cạn kiệt, và chỉ còn nguồn năng lượng duy nhất là protein, thời điểm này, kho protein dự trữ một lần nữa bước vào giai đoạn suy giảm nhanh chóng.
Biên tập viên: Trần Tiến Phong
Đánh giá: Trần Trà My, Trần Phương Phương
Gầy mòn
Gầy mòn ngược lại với béo phì và đặc trưng bởi sự sụt cân trầm trọng. Nó được gây ra bởi sự thiếu hụt thực phẩm hoặc tình trạng bệnh lý làm giảm sự ngon miệng, bao gồm các rối loạn tâm lý, bất thường vùng hạ đồi, và các yếu tố giải phóng từ mô ngoại vi. Trong nhiều trường hợp, đặc biệt là những người có bệnh nặng như ung thư, giảm ngon miệng có thể phối hợp với tăng tiêu thụ năng lượng, hậu quả là sụt cân nghiêm trọng.
Chán ăn được định nghĩa như là giảm lượng thực phẩm ăn vào chủ yếu do giảm ngon miệng, trái ngược với định nghĩa thông thường là “không ăn”. Định nghĩa này nhấn mạnh tầm quan trọng của các cơ chế thần kinh trung ương trong bệnh sinh của chán ăn ở các bệnh như ung thư, hoặc khi các vấn đề phổ biến khác, như là đau và buồn nôn, cũng có thể làm cho một người tiêu thụ ít thực phẩm hơn. Chán ăn tâm thần là một trạng thái tâm lý bất thường trong đó một người mất tất cả hứng thú với thức ăn thậm chí buồn nôn vì thực phẩm; hậu quả dẫn đến gầy mòn trầm trọng.
Suy kiệt là một bệnh lý chuyển hóa trong đó tăng năng lượng tiêu thụ dẫn đến giảm cân nhiều hơn là do ăn ít đơn thuần. Chán ăn và suy kiệt thường xảy ra đồng thời ở nhiều bệnh ung thư hoặc trong “hội chứng suy mòn” quan sát ở những bệnh nhân bị hội chứng suy giảm miễn dịch mắc phải (AIDS) và bệnh viêm mạn tính. Hầu hết các loại ung thư gây ra cả chán ăn và suy kiệt, và hội chứng suy kiệt - chán ăn phát triển ở hơn một nửa số bệnh nhân ung thư trong quá trình mắc bệnh của mình.
Thần kinh trung ương và các yếu tố ngoại vi được cho là đóng góp vào sự gia tăng chán ăn và suy kiệt ở bệnh ung thư. Nhiều cytokines viêm, bao gồm các yếu tố hoại tử u factor-α, interleukin-6, interleukin-1β, và yếu tố phân giải protein, được chỉ ra là gây chán ăn và suy kiệt. Phần lớn các cytokines viêm xuất hiện để giải quyết chán ăn bằng cách hoạt hóa hệ thống melanocortin ở vùng hạ đồi. Cơ chế chính xác mà các cytokin hoặc sản phẩm của u tương tác với con đường melanocortin để giảm sự ăn uống chưa rõ ràng, nhưng việc phong tỏa các melanocortin receptors ở vùng dưới đồi xuất hiện hầu như ngăn cản chán ăn và hậu quả suy kiệt ở động vật thực nghiệm. Mặc dù vậy, các nghiên cứu bổ sung là cần thiết để hiểu biết rõ hơn về cơ chế sinh bệnh học chán ăn và suy kiệt ở những bệnh nhân ung thư cũng như phát triển các liệu pháp để cải thiện tình trạng dinh dưỡng và sự sống của người bệnh.
Chán ăn và suy nhược
Sự suy giảm dự trữ các chất trong các mô khi bị thiếu đói. Mặc dù các mô thích dùng carbohydrate hơn là chất béo hay protein để có năng lượng, số lượng carbohydrate bình thường dự trữ trong toàn cơ thể chỉ là vài trăm grams (chủ yếu là glycogen trong gan và cơ), và nó chỉ đủ cung cấp nhu cầu năng lượng cho các hoạt động của cơ thể trong vòng nửa ngày. Do đó, ngoại trừ trong vài giờ đầu, hậu quả chủ yếu của thiếu ăn là sự sụt giảm mô mỡ và protein. Bởi vì chất béo là nguồn năng lượng chính (100 lần nhiều hơn năng lượng carbohydrate được dữ trữ ở người bình thường), tỷ lệ sụt giảm chất béo không hề thấp đi, cho đến khi hầu hết chất béo trong cơ thể đã cạn kiệt.
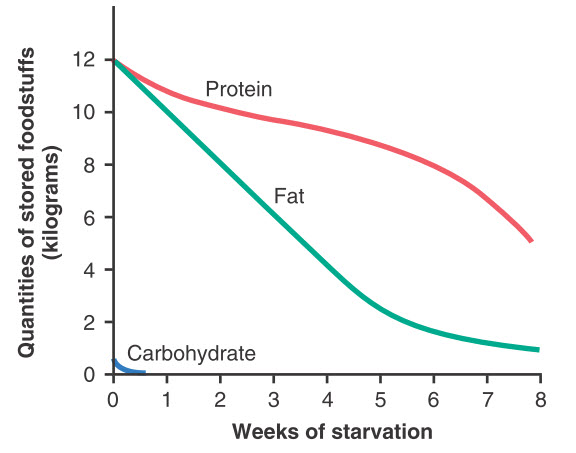
Hình. Ảnh hưởng của đói đến dự trữ thức ăn của cơ thể.
Protein trải qua ba giai đoạn suy giảm: giảm nhanh trong giai đoạn đầu tiên, tiếp theo là sự giảm chủ yếu nhưng chậm, và cuối cùng lại giảm nhanh trong một thời gian ngắn trước khi tử vong. Sự giảm nhanh ban đầu là do sử dụng dễ dàng protein được huy động cho chuyển hóa trực tiếp hoặc chuyển thành glucose và sau đó glucose được chuyển hóa chủ yếu bởi não. Sau khi nguồn dự trữ protein được huy động được dùng hết sau giai đoạn sớm của thiếu ăn, phần protein còn lại không dễ dàng được giải phóng. Thời điểm này, tỷ lệ tân tạo glucose giảm từ 1/3 đến 1/5 so với trước đó, và tỷ lệ suy giảm protein cũng trở nên thấp hơn đáng kể. Sự thiếu hụt glucose sẵn có khởi đầu một loạt các sự kiện dẫn đến sử dụng chất béo quá mức và chuyển đổi một số sản phẩm giáng hóa chất béo thành thể ketone, chẳng hạn sản xuất ketosis. Thể ketone, giống như glucose, có thể đi qua hàng rào máu não và được tế bào não sử dụng để cung cấp năng lượng. Do đó, khoảng hai phần ba năng lượng não sử dụng có nguồn gốc từ các thể ketone, chủ yếu từ β-hydroxybutyrate. Chuỗi sự kiện này giúp bảo toàn một phần kho protein dự trữ của cơ thể.
Cuối cùng đến lúc kho dự trữ chất béo hoàn toàn cạn kiệt, và chỉ còn nguồn năng lượng duy nhất là protein. Thời điểm này, kho protein dự trữ một lần nữa bước vào giai đoạn suy giảm nhanh chóng. Bởi vì protein là sống còn để duy trì chức năng tế bào, cái chết sẽ đến khi protein trong cơ thể chỉ còn một nửa so với mức bình thường.
Thiếu hụt vitamin trong thiếu đói. Kho dự trữ một số loại vitamins, đặc biệt là vitamin tan trong nước - vitamin nhóm B vitamin C - không thể duy trì lâu dài trong khi thiếu ăn. Do đó, sau một hoặc vài tuần thiếu đói, sự thiếu hụt vitamin nhẹ bắt đầu xuất hiện và sau nhiều tuần, thiếu hụt vitamin trầm trọng sẽ xảy ra. Những thiếu hụt này có thể góp phần tăng sự suy kiệt dẫn đến tử vong.
Bài viết cùng chuyên mục
Sinh lý bệnh của bệnh đần độn
Thiếu hụt bẩm sinh tuyến giáp, tuyến giáp không có khả năng sản xuất hormon giáp do khiếm khuyết một gen của tuyến, hoặc do thiếu hụt iod trong chế độ ăn.
Kiểm soát sự bài tiết Canxi của thận
Tái hấp thu canxi tương tự như đối với natri, sự bài tiết canxi được điều chỉnh để đáp ứng nhu cầu của cơ thể, khi tăng lượng canxi ăn vào, cũng làm tăng bài tiết canxi qua thận. Canxi vừa được lọc vừa tái hấp thu ở thận nhưng không được bài tiết ra ngoài. Do đó, tốc độ bài tiết canxi qua thận...
Viêm nhiễm: sự đáp ứng của đại thực bào và bạch cầu hạt trung tính
Đại thực bào có thể thực bào nhiều vi khuẩn hơn (khoảng gấp 5 lần) và các phần tử lớn hơn, bao gồm cả bạch cầu hạt trung tính. Đại thực bào cũng đóng vai trò quan trọng trong việc khởi động sản xuất kháng thể.
Chuyển hóa sắt: tổng hợp hemoglobin
Khi hồng cầu bị phá hủy, các hemoglobin từ các tế bào này được đưa vào các tế bào monocytemacrophage. Sắt giải phóng và được lưu trữ chủ yếu trong ferritin được sử dụng khi cần thiết cho sự hình thành của hemoglobin mới.
Loạn thị: rối loạn độ hội tụ của mắt
Loạn thị là tình trạng độ hội tụ của mắt bị rối loạn gây nên sự khác nhau về khả năng hội tụ của mắt trên các mặt phẳng vuông góc với nhau.
Điều chỉnh trao đổi dịch và cân bằng thẩm thấu dịch trong và ngoài tế bào
Sự trao đổi giữa dịch nội bào và ngoại bào chủ yếu dựa vào chênh lêch áp suất thẩm thấu của những chất tan như Na, K, Cl.
Cân bằng thẩm thấu được duy trì giữa dịch nội và ngoại bào
Nếu dung dịch muối đẳng trương được đưa vào ngoại bào thì nồng độ thẩm thấu sẽ không đổi, chỉ có thể tích dịch ngoại bào tăng lên.
Điều tiết và độ mở của đồng tử: điều hòa tự động thần kinh tự động của mắt
Hệ giao cảm phân phối cho mắt bắt nguồn từ các tế bào sừng bên giữa trước ở đốt tủy ngực đầu tiên. Từ đó, các sợi giao cảm đi đến chuỗi hạch giao cảm và đi lên hạch cổ trên, nơi chúng xi náp với các neuron sau hạch.
Vai trò của Cholesterol và Lipoprotein trong xơ vữa động mạch
Yếu tố quan trọng gây xơ vữa động mạch là nồng độ LDLs cholesterol trong máu cao, LDLs cholesterol trong huyết tương cao, tăng lên do nhiều yếu tố, đặc biệt là do ăn nhiều chất béo bão hòa.
Các loại tế bào bạch cầu: sáu loại bạch cầu bình thường có mặt
Sáu loại bạch cầu bình thường có mặt trong máu: bạch cầu đa nhân trung tính, bạch cầu đa nhân ưa acid, bạch cầu đa nhân ưa base, tế bào mono, lympho bào, và đôi khi có tương bào.
Đông máu nội mạch rải rác: tắc nghẽn mạch máu nhỏ ở ngoại vi
Sự tắc nghẽn các mạch máu nhỏ ngoại vi sẽ ngăn cản mô nhận oxy và các chất dinh dưỡng khác, điều này sẽ dẫn đến hoặc làm nặng thêm tình trạng shock tuần hoàn.
Bạch cầu ưa base (bạch cầu ái kiểm): vai trò quan trọng trong phản ứng dị ứng
Dưỡng bào và bạch cầu ái kiềm đóng một vai trò quan trọng trong nhiều loại phản ứng dị ứng bởi lọai kháng thể gây ra phản ứng dị ứng, IgE có xu hướng đặc biệt gắn với dưỡng bào và bạch cầu ái kiềm.
Dịch ngoại bào: phân bố dịch giữa khoảng kẽ và mạch máu
Thể tích dịch ngoại bào và thể tích máu thường được kiểm soát đồng thời, nhưng số lượng phân phối dịch giữa kẽ và máu phụ thuộc vào các đặc tính vật lý của tuần hoàn và khoảng kẽ, cũng như động lực của quá trình trao đổi dịch qua các màng mao mạch.
Tăng mức lọc cầu thận: tăng hệ số lọc mao mạch cầu thận
Mặc dù tăng Kf kéo theo tăng mức lọc cầu thận và giảm Kf, làm giảm mức lọc cầu thận, nhưng thay đổi Kf hầu như chắc chắn không là cơ chế tiên phát cho việc điều chỉnh mức lọc cầu thận hàng ngày bình thường.
Khí ra vào phổi: áp lực gây ra sự chuyển động của không khí
Áp suất màng phổi là áp lực của dịch trong khoang mỏng giữa màng phổi lá tạng và màng phổi lá thành. Áp lực này bình thường hút nhẹ hay áp lực âm nhẹ.
Bệnh van hai lá: huyết động học trong hẹp và hở van
Khi áp lực tâm nhĩ trái tăng lên, máu bắt đầu dồn lên phổi, cuối cùng trở lại động mạch phổi. Ngoài ra, phù nề phổi ngay từ đầu gây co thắt tiểu động mạch phổi.
Đại cương về viêm
Virchow (thế kỷ XIX) đã cho rằng viêm là phản ứng cục bộ, nhưng hiện tại người ta cho rằng viêm là biểu hiện cục bộ của một phản ứng toàn thân.
Shock giảm khối lượng tuần hoàn do mất huyết tương
Shock giảm thể tích do mất huyết tương có các đặc điểm gần giống với shock do xuất huyết, ngoại trừ một yếu tố phức tạp khác.
Béo phì: sự lắng đọng chất béo dư thừa
Di truyền ảnh hưởng tới trung tâm não điều hòa năng lượng hay những con đường mà kiểm soát năng lượng sử dụng hoặc năng lượng được dự trữ có thể là nguyên nhân gây ra béo phì di truyền ở người.
Kiểm soát sự bài tiết magie qua thận và nồng độ ion magie ngoại bào
Điều chỉnh bài tiết magie được thực hiện chủ yếu bằng cách thay đổi tái hấp thu ở ống thận. Ống lượn gần thường chỉ tái hấp thu khoảng 25% lượng magie đã lọc.
Angiotensin II: vai trò trong việc kiểm soát bài tiết của thận
Khi lượng natri giảm xuống dưới mức bình thường, nồng độ Angiotensin II tăng lên gây giữ natri và nước, đồng thời chống lại việc giảm huyết áp động mạch nếu không xảy ra.
Suy tim trái: nghẽn mạch phổi và phù phổi
Khi tim trái suy mà tim phải bình thường, máu tiếp tục được tống lên phổi nhờ tim phải, trong khi nó không được bơm ra khỏi phổi nhờ tim trái vào tuần hoàn hệ thống.
Trong ống thận: HCO3- được lọc sau đó tái hấp thu bởi sự tương tác với H+
Quá trình tái hấp thu này được khởi đầu bởi một phản ứng trong ống thận giữa HCO3- được lọc ra ở cầu thận và H+ được bài tiết bởi tế bào thành ống thận.
Sự thực bào: chức năng của bạch cầu hạt trung tính và đại thực bào
Ngoài việc tiêu hóa vi khuẩn ăn vào trong phagosome thì bạch cầu hạt trung tính và đại thực bào còn chứa các tác nhân diệt khuẩn giết được hầu hết vi khuẩn kể cả khi enzym của lysosome không tiêu hóa được chúng.
Bệnh thận: tổn thương thận cấp và bệnh thận mạn
Trong phạm vi 2 phân loại, có rất nhiều các bệnh thận cụ thể có thể ảnh hưởng đến các mạch máu thận, cầu thận, ống thận, kẽ thận, các bộ phận của đường tiết niệu bên ngoài thận bao gồm cả niệu quản và bàng quang.
