- Trang chủ
- Sách y học
- Bài giảng sinh lý bệnh
- Kiểm soát áp suất thẩm thấu và nồng độ natri: cơ chế osmoreceptor-ADH và cơ chế khát
Kiểm soát áp suất thẩm thấu và nồng độ natri: cơ chế osmoreceptor-ADH và cơ chế khát
Trong trường hợp không có các cơ chế ADH-khát, thì không có cơ chế feedback khác có khả năng điều chỉnh thỏa đáng nồng độ natri huyết tương và áp suất thẩm thấu.
Biên tập viên: Trần Tiến Phong
Đánh giá: Trần Trà My, Trần Phương Phương
Ở một người khỏe mạnh, các cơ chế osmoreceptor-ADH và cơ chế khát làm việc song song để điều chỉnh một cách chính xác áp suất thẩm thấu dịch ngoại bào và nồng độ natri, bất chấp những thách thức liên tục của tình trạng mất nước. Ngay cả với những thách thức thêm vào, chẳng hạn như lượng muối vào cao, các hệ thống feedback này có năng lực giữ độ thẩm thấu huyết tương hợp lý không đổi. Hình cho thấy rằng một sự gia tăng lượng natri vào cao bằng 6 lần bình thường chỉ có một ảnh hưởng nhỏ đến nồng độ natri huyết tương trong khi các cơ chế ADH và cơ chế khát đều hoạt động bình thường.
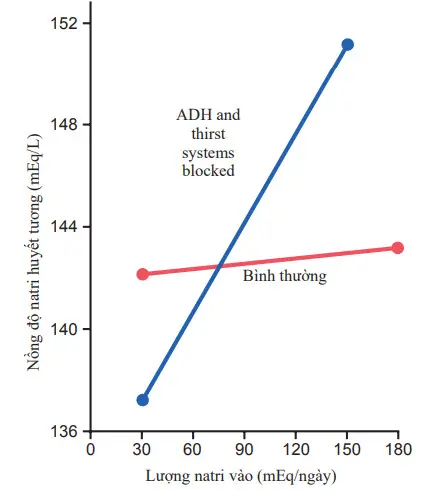
Hình. Ảnh hưởng của những thay đổi lớn về lượng natri ăn vào đối với nồng độ natri trong dịch ngoại bào ở chó trong điều kiện bình thường (đường màu đỏ) và sau khi hệ thống phản hồi cơn khát và hormone chống bài niệu (ADH) bị chặn (đường màu xanh). Lưu ý rằng việc kiểm soát nồng độ natri trong dịch ngoại bào kém khi không có các hệ thống phản hồi này.
Khi 1 trong 2 cơ chế hoặc cơ chế ADH hoặc cơ chế khát suy yếu, thì cơ chế còn lại thông thường vẫn có thể kiểm soát áp suất thẩm thấu ngoại bào và nồng độ natri với hiệu quả hợp lý, miễn là có đủ lượng dịch vào để cân bằng với khối lượng nước tiểu bắt buộc hàng ngày và sự mất nước gây ra bởi sự hô hấp, sự ra mồ hôi, hoặc đường tiêu hóa. Tuy nhiên, nếu cả hai cơ chế ADH và cơ chế khát thất bại đồng thời, thì nồng độ natri huyết tương và áp suất thẩm thấu khó được khó kiểm soát; do đó, khi lượng natri vào tăng lên sau khi ngăn chặn toàn bộ hệ thống ADH-khát, thì có những thay đổi tương đối lớn trong nồng độ natri huyết tương xảy ra.
Trong trường hợp không có các cơ chế ADH-khát, thì không có cơ chế feedback khác có khả năng điều chỉnh thỏa đáng nồng độ natri huyết tương và áp suất thẩm thấu.
Vai trò của angiotensin II và aldosteron trong kiểm soát áp suất thẩm thấu dịch ngoại bào và nồng độ natri
Cả angiotensin II và aldosterone đóng một vai trò quan trọng trong việc điều chỉnh sự tái hấp thu natri bởi các ống thận. Khi lượng natri vào thấp, làm tăng nồng độ của các hormone này kích thích sự tái hấp thu natri bởi thận và do đó ngăn ngừa sự sự mất mát lớn natri, mặc dù lượng natri vào có thể giảm xuống thấp tới 10% so với bình thường. Ngược lại, với lượng natri vào cao, làm giảm sự hình thành của các hormone này cho phép thận bài xuất một lượng lớn natri.
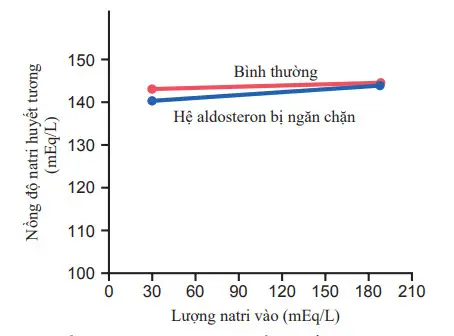
Hình. Ảnh hưởng của những thay đổi lớn về lượng natri ăn vào đối với nồng độ natri trong dịch ngoại bào ở chó trong điều kiện bình thường (vạch đỏ) và sau khi hệ thống phản hồi aldosteron bị chặn (vạch xanh). Lưu ý rằng nồng độ natri được duy trì tương đối ổn định trong phạm vi lượng natri lớn này, có hoặc không có kiểm soát phản hồi aldosterone.
Bởi vì tầm quan trọng của angiotensin II và aldosteron trong việc điều chỉnh sự bài xuất natri bởi thận, một người có thể suy luận sai lầm rằng chúng cũng đóng một vai trò quan trọng trong việc điều chỉnh nồng độ natri dịch ngoại bào. Mặc dù các hormone này làm tăng một lượng natri trong dịch ngoại bào, chúng cũng làm tăng thể tích dịch ngoại bào bằng cách gia tăng sự tái hấp thu nước cùng với natri. Do đó, angiotensin II và aldosteron có ít ảnh hưởng đến nồng độ natri, ngoại trừ dưới những điều kiện khắc nghiệt.
Sự không quan trọng tương đối này của aldosterone trong việc điều chỉnh nồng độ natri dịch ngoại bào được thể hiện bởi thí nghiệm trong hình. Hình này cho thấy sự ảnh hưởng lên nồng độ natri huyết tương của những thay đổi lượng natri vào nhiều hơn gấp sáu lần với hai điều kiện: (1) dưới các điều kiện bình thường và (2) sau khi hệ thống feedback aldosterone bị chặn lại bằng cách loại bỏ các tuyến thượng thận và truyền cho các động vật aldosterone ở một tốc độ không đổi sao cho nồng độ huyết tương không thể tăng hoặc giảm. Lưu ý rằng khi lượng natri vào đã tăng gấp sáu lần, nồng độ huyết tương thay đổi chỉ khoảng 1-2% trong cả hai trường hợp. Sự phát hiện này cho thấy rằng thậm chí không có một hệ thống feedback chức năng aldosterone, nồng độ natri huyết tương có thể được điều chỉnh tốt. Các thí nghiệm cùng loại đã được tiến hành sau khi ngăn chặn sự hình thành angiotensin II, cho kết quả tương tự.
Có hai lý do chính giải thích tại sao những thay đổi của angiotensin II và aldosteron không có một ảnh hưởng lớn đến nồng độ natri huyết tương. Thứ nhất, như đã thảo luận trước đó, angiotensin II và aldosteron làm tăng cả sự tái hấp thu natri và sự tái hấp thu nước bởi các ống thận, dẫn đến làm tăng khối lượng dịch ngoại bào và số lượng natri nhưng ít thay đổi nồng độ natri. Thứ hai, miễn là cơ chế ADH-khát có chức năng, bất cứ khuynh hướng nào thiên về gia tăng nồng độ natri huyết tương được đền bù bằng cách gia tăng lượng nước vào hoặc gia tăng sự bài tiết ADH huyết tương, điều đó có xu hướng pha loãng dịch ngoại bào trở về bình thường. Hệ thống ADH-khát làm lu mờ nhiều các hệ thống angiotensin II và aldosteron trong điều hoà nồng độ natri dưới những điều kiện bình thường. Ngay cả ở những bệnh nhân cường aldosteron nguyên phát, những người có mức aldosterone vô cùng cao, nồng độ natri huyết tương thường xuyên tăng chỉ khoảng 3-5 mEq / L trên mức bình thường.
Dưới những điều kiện khắc nghiệt gây ra bởi sự mất hoàn toàn của sự bài tiết aldosterone giống như kết quả của sự cắt bỏ tuyến thượng thận hoặc ở các bệnh nhân bị bệnh Addison (suy giảm nghiêm trọng sự bài tiết hoặc thiếu toàn bộ aldosterone), có sự mất mát to lớn natri qua thận, điều đó có thể dẫn đến sự suy giảm nồng độ natri huyết tương. Một trong những lý do cho điều này là sự mất mát lớn này của natri cuối cùng gây ra sự suy kiệt nghiêm trọng thể tích dịch và làm giảm huyết áp, điều này có thể kích hoạt cơ chế khát thông qua các phản xạ tim mạch. Sự kích hoạt này dẫn đến một sự pha loãng hơn nữa của nồng độ natri trong huyết tương, mặc dù sự gia tăng lượng nước vào giúp giảm đến mức tối thiểu sự sụt giảm thể tích dịch cơ thể trong những điều kiện này.
Do đó, những tình huống cực độ là tồn tại trong đó nồng độ natri huyết tương có thể thay đổi đáng kể, ngay cả với một cơ chế chức năng ADH-khát. Mặc dù vậy, cơ chế ADH-khát cho đến nay là hệ thống feedback mạnh mẽ nhất trong cơ thể trong kiểm soát áp suất thẩm thấu dịch ngoại bào và nồng độ natri.
Cơ chế thèm muối trong kiểm soát nồng độ natri dịch ngoại bào và thể tích dịch ngoại bào
Sự duy trì thể tích dịch ngoại bào và nồng độ natri bình thường đòi hỏi một sự cân bằng giữa sự bài xuất natri và lượng natri vào. Trong những nền văn minh hiện đại, lượng natri vào là hầu như luôn luôn lớn hơn mức cần thiết cho sự cân bằng nội môi. Trong thực tế, lượng natri vào trung bình cho một người trong các nền văn hóa công nghiệp hóa, người ăn các thực phẩm đã chế biến, thường khoảng giữa 100 và 200 mEq / ngày, mặc dù con người có thể tồn tại và hoạt động bình thường trong khi sự nhập vào chỉ 10 đến 20 mEq / ngày. Vì vậy, hầu hết mọi người ăn quá nhiều natri hơn mức cần thiết cho sự cân bằng nội môi, và bằng chứng chỉ ra rằng lượng natri vào cao thường xuyên của chúng ta có thể góp phần vào các rối loạn tim mạch như cao huyết áp.
Sự thèm muối là do một phần trong thực tế các loài động vật và con người thích muối và ăn nó bất kể họ có thiếu muối hay không. Sự thèm muối cũng có một thành phần điều hoà trong đó có một đợt vận động hành vi để thu được muối khi một sự thiếu hụt natri tồn tại trong cơ thể. Sự vận động hành vi này là đặc biệt quan trọng trong các động vật ăn cỏ, chúng vốn ăn một chế độ ăn ít natri, nhưng sự thèm muối cũng có thể quan trọng ở những người có một sự thiếu hụt nghiêm trọng natri, chẳng hạn như xảy ra trong bệnh Addison. Trong trường hợp này, có một sự thiếu hụt bài tiết aldosterone, điều đó gây ra sự mất mát quá mức natri trong nước tiểu và dẫn đến giảm thể tích dịch ngoại bào và giảm nồng độ natri; cả những thay đổi này gợi ra sự thèm muối.
Nói chung, các kích thích chính làm tăng sự thèm muối có liên quan với sự thiếu hụt natri và sự giảm thể tích máu hay sự giảm huyết áp liên quan đến sự suy tuần hoàn.
Cơ chế thần kinh cho sự thèm muối tương tự với cơ chế khát. Một số trong những trung tâm thần kinh tương tự nhau ở khu vực AV3V của não bộ dường như có liên quan bởi vì những tổn thương trong khu vực này thường xuyên ảnh hưởng đến cả sự khát nước và sự thèm muối đồng thời ở động vật. Ngoài ra, các phản xạ tuần hoàn được gợi ra bởi huyết áp thấp hoặc sự giảm khối lượng máu ảnh hưởng đến cả sự khát nước và sự thèm muối tại cùng một thời điểm.
Bài viết cùng chuyên mục
Đặc tính của lympho T: hoạt hóa tế bào T và miễn dịch trung gian tế bào
Tế bào T đi vào tuần hoàn và được phân bố khắp cơ thể, đi qua thành mao mạch vào các khoảng gian bào, trở lại vào bạch huyết và máu một lần nữa, và tuần hoàn một lần nữa và một lần nữa trên khắp cơ thể.
Cân bằng natri và dịch trong cơ thể: tầm quan trọng của natri và áp lực bài niệu
Bài tiết áp lực đề cập đến tác động của huyết áp tăng lên để tăng bài tiết khối lượng nước tiểu, trong khi bài tiết natri áp lực đề cập đến sự gia tăng bài tiết natri xảy ra với huyết áp cao.
Tổn thương thận cấp tại thận: nguyên nhân do các bất thường tại thận
Tổn thương thận cấp tại thận có thể chia thành các nhóm sau: tình trạng tổn thương các mao mạch cầu thận hoặc các mạch nhỏ của thận, tình trạng tổn thương biểu mô ống thận, và tình trạng gây tổn thương kẽ thận.
Phì đại tim: xẩy ra ở bệnh van tim và tim bẩm sinh
Phì đại tim thường được coi là phản ứng bù trừ của tim đối với khối lượng công việc tăng lên và thường có lợi cho việc duy trì cung lượng tim khi đối mặt với những bất thường làm giảm hiệu quả hoạt động của tim.
Phân tích biểu đồ suy tim cung lượng cao
Nếu tập thể dục, sẽ có dự trữ tim ít do khả năng của tim đã đạt được mức gần cực đại để bơm thêm lượng máu qua lỗ thông động tĩnh mạch. Tình trạng này được gọi là suy tim cung lượng cao.
Cơ chế điều hòa nồng độ H+: hệ thống đệm phổi thận
Khi có sự thay đổi nồng độ H+, các hệ thống đệm trong dịch cơ thể sẽ phản ứng ngay trong vòng vài giây để giảm thiểu sự thay đổi này. Hệ thống đệm không thể loại bỏ H+ hoặc thêm H+ cho cơ thể.
Hấp thụ và bài tiết natri: được cân bằng trong trạng thái ổn định
Nếu rối loạn chức năng thận không quá nghiêm trọng, có thể đạt được cân bằng natri chủ yếu bằng cách điều chỉnh nội thận với những thay đổi tối thiểu về thể tích dịch ngoại bào hoặc các điều chỉnh toàn thân khác.
Bệnh thận mạn: nguyên nhân do mạch máu thận
Ngay cả ở những người khỏe mạnh không có tăng huyết áp hay đái tháo đường tiềm ẩn, lượng huyết tương qua thận và mức lọc cầu thận (GFR) sẽ giảm 40-50% khi đến tuổi 80.
Sinh lý bệnh soi sáng công tác dự phòng và điều trị
Sự hiểu biết về vai trò của nguyên nhân và điều kiện gây bệnh sẽ giúp cho việc đề ra kế hoạch phòng bệnh đúng.
Đông máu cầm máu: các xét nghiệm sử dụng trong lâm sàng
Máu lấy từ bệnh nhân ngay lập tức hòa trộn với oxalat nên không xảy ra quá trình chuyển hóa prothrombin thành thrombin. Sau đó, một lượng lớn ion calci và yếu tố mô nhanh chóng được hòa trộn với máu có oxalat.
Một số vấn đề quan trọng trong bệnh sinh học
Cục bộ và toàn thân: một tổn thương tại chỗ, gây nên bất cứ do yếu tố bệnh nguyên nào, xét cho cùng cũng sẽ ảnh hưởng đến toàn thân.
Hệ thống đệm H+ trong dịch cơ thể
Tầm quan trọng của hệ thống đệm được thể hiện rõ khi nồng độ H+ thấp trong các dịch cơ thể và lượng tương đối lớn acid được sản xuất ra trong cơ thể.
Sinh lý bệnh gan nhiễm mỡ
Nhìn chung biểu hiện lâm sàng thường kín đáo và tiến triển thường nhẹ, vì mỡ không phải là chất độc, nó chỉ gây ra tác động cơ học là gan hơi lớn.
Đại cương rối loạn cân bằng acid base
Hầu hết các phản ứng chuyển hóa xảy ra trong cơ thể luôn đòi hỏi một pH thích hơp, trong khi đó phần lớn các sản phẩm chuyển hóa của nó.
Hiệu chỉnh loạn thị bằng kính trụ: sử dụng hai kính trụ với độ hội tụ khác nhau
Sau khi thử vài thấu kính cầu khác nhau trước mắt loạn thị, mỗi độ hội tụ của thấu kính làm hội tụ rõ nét một vài các thanh song song nhau nhưng sẽ không rõ một vài các thanh khác vuông góc với các thanh sắc nét đó.
Bất thường bài tiết hormone tăng trưởng (GH)
Bất thường bài tiết hormone tăng trưởng gây ra suy tuyến yên trước, chứng lùn, bệnh khổng lồ, bệnh to cực chi, suy tuyến yên trước ở người trưởng thành.
Các đặc trưng trong trạng thái sốt
Khi điểm nhiệt chuẩn của trung tâm điều nhiệt đột ngột thay đổi từ mức bình thường lên mức cao hơn, thân nhiệt sẽ phải mất nhiều giờ để đạt được điểm nhiệt chuẩn mới.
Vận chuyển nước và các chất ở quai Henle của thận
Đoạn dày của ngành lên quai Henle hầu như không thấm nước. Do đó, hầu hết nước qua đoạn này vẫn ở lại trong lòng ống mặc dù có một lượng lớn chất tan được tái hấp thu.
Macula Densa natri clorua giảm gây ra sự giãn nở của các tiểu động mạch liên quan và tăng giải phóng Renin
Renin giải phóng từ các tế bào này sau đó có chức năng như một loại enzyme để tăng sự hình thành của angiotensin I, được chuyển thành angiotensin II.
Tăng thông khí phổi: giảm nồng độ H+ dịch ngoại bào và làm tăng pH
Nếu chuyển hóa tạo CO2 vẫn không đổi, chỉ có các yếu tố ảnh hưởng đến pCO2 trong dịch ngoại bào là tốc độ thông khí ở phổi. Thông khí phế nang càng cao, pCO2 càng thấp.
Sơ lược sự phát triển về khái niệm bệnh
Bệnh là do rối loạn các thể dịch đó. Ví dụ: có quá nhiều dịch nhầy ở khắp nơi như ở phổi , ở ổ bụng, ở ruột, ở trực tràng
Tồn tại ống động mạch: bệnh tim bẩm sinh shunt trái phải
Ngay sau khi trẻ được sinh ra và bắt đầu thở, phổi sẽ phồng lên, các phế nang chứa đầy không khí mà sức cản của dòng máu qua cây mạch phổi cũng giảm rất nhiều, tạo điều kiện cho áp lực động mạch phổi giảm xuống.
Rối loạn dạ dày trong quá trình tiêu hóa
Viêm dạ dày thường gây ra bởi sự nhiễm khuẩn mạn tính niêm mạc dạ dày, tình trạng này có thể chữa khỏi hoàn toàn bới một liệu trình kháng sinh cường độ lớn.
Điều trị suy thận: ghép thận hoặc lọc máu với thận nhân tạo
Lọc máu không thể duy trì hoàn toàn bình thường các thành phần dịch cơ thể và không thể thay thế hoàn toàn các chức năng phức tạp của thận, sức khỏe của bệnh nhân vẫn bị suy giảm đáng kể.
Sự hình thành bạch cầu: quá trình hình thành trong tủy xương
Bạch cầu được hình thành trong tủy xương được dự trữ trong tủy xương đến khi chúng cần thiết phải đi vào hệ tuần hoàn. Sau đó, khi có nhu cầu, các yếu tố khác nhau làm cho chúng được giải phóng.
