- Trang chủ
- Sách y học
- Bài giảng miễn dịch
- Thiếu hụt miễn dịch thứ phát
Thiếu hụt miễn dịch thứ phát
Biên tập viên: Trần Tiến Phong
Đánh giá: Trần Trà My, Trần Phương Phương
Nguyên nhân của thiếu hụt miễn dịch thứ phát
Nguyên nhân gây thiếu hụt miễn dịch thứ phát phổ biến hơn nhiều so với thiếu hụt tiên phát. Bởi vì chức năng hoạt động của các thành phần của hệ miễn dịch phụ thuộc vào sự cân bằng giữa sự tổng hợp và sự thóai hóa chúng nên sự thiếu hụt thứ phát sẽ xảy ra khi sự tổng hợp kém đi hoặc sự thoái hóa tăng lên.
Sự mất protein của cơ thể có thể dẫn đến giảm gammaglobulin máu. Đó là trường hợp thường gặp của hội chứng thận hư (gây mất protein qua đường thận) và các bệnh lý ruột gây mất protein. Sự mất protein trong bệnh thận thường có tính chọn lọc, do đó ta có thể thấy rằng lượng IgM vẫn bình thường còn IgG thì giảm rõ. Trong bệnh lý ruột, mất protein có thể gặp trong một số bệnh như bệnh Crohn, viêm đại tràng loét và bệnh celiac. Trong bệnh cảnh giãn bạch mạch đường ruột, ta có thể thấy mất cả tế bào lymphô lẫn protein.
Hình ảnh giảm sinh tổng hợp có thể thấy rõ trong suy dinh dưỡng protein – năng lượng. Thiếu hụt protein dẫn đến biến đổi sâu sắc ở các cơ quan trong cơ thể kể cả hệ miễn dịch. Trong trường hợp này chúng ta có thể thấy giảm khả năng sản xuất kháng thể khi cơ thể được gây miễn dịch, đồng thời, miễn dịch tế bào, chức năng thực bào và hoạt tính bổ thể cũng thay đổi. Thiếu hụt miễn dịch do nguyên nhân này có thể hồi phục trong một số trường hợp khi cơ thể được bù đầy đủ protein và calo.
Bệnh nhân bị bệnh tăng sinh lymphô có xu hướng rất dễ nhiễm trùng. Sự xuất hiện thường xuyên của nhiễm trùng cơ hội trên những người bị ung thư lan tỏa đã nói lên tình trạng bị suy giảm miễn dịch khá nặng nề do hậu quả ức chế của bệnh hoặc do điều trị. Bệnh bạch cầu lympho mạn tính thường đi kèm với giảm gammaglobulin máu và nhiễm trùng hô hấp tái phát nhiều lần và điều này đã làm cho bệnh ngày càng nặng dần nhanh chóng. Có trường hợp nếu ta cho bù immunoglobulin thì bệnh sẽ cải thiện. U lympho non-Hodgkin có thể đi kèm với thiếu hụt miễn dịch cả thể dịch lẫn tế bào; lượng Ig vẫn bình thường cho đến giai đoạn muộn của bệnh. Hầu hết các bệnh nhân đa u tủy đều có giảm Ig đa clôn, nhưng lại tăng Ig đơn clôn một cách rất đặc trưng.
Các thuốc ức chế miễn dịch tác động lên rất nhiều khâu của chức năng tế bào. Chức năng của lymphô bào và bạch cầu múi thường giảm. Rất ít khi có giảm gammaglobulin nặng. Bệnh nhân dùng thuốc ức chế miễn dịch trong quá trình điều trị ung thư hoặc bảo vệ mảnh ghép thường rất dễ bị nhiễm trùng cơ hội.
Chúng ta cũng nên lưu ý rằng một số kháng sinh cũng có tác dụng ức chế miễn dịch. Đó là kháng sinh có cấu trúc hóa học giống các thuốc chống chuyển hóa và gây độc tế bào. Ví dụ như gentamicin, amikacin và tobramycin có thể làm giảm khả năng hóa hướng động đối với tế bào trung tính; cotrimoxazole, rifampicin và tetracycline có thể làm biến đổi miễn dịch tế bào; chloramphenicol, cotrimoxazole và rifampicin làm thay đổi đáp ứng kháng thể sơ cấp và thứ cấp.
Trong nhiều bệnh nhiễm trùng, vi sinh vật có khả năng ức chế miễn dịch hơn là kích thích miễn dịch. Người ta đã lưu ý thấy điều này xảy ra nặng nề, mặc dù chỉ thóang qua, trong nhiều bệnh nhiễm trùng virus, nhất là cytomegalovirus, sởi, rubella, đơn nhân nhiễm khuẩn và viêm gan virus và trong một số nhiễm trùng vi khuẩn như lao, brucellosis, phong và giang mai: tuy nhiên, ví dụ rõ nét nhất là bệnh cảnh mới được phát hiện trong những năm gần đây, đó là hội chứng thiếu hụt miễn dịch mắc phải (AIDS).
Hội chứng thiếu hụt miễn dịch mắc phải (AIDS)
Hội chứng thiếu hụt miễn dịch mắc phải (Aquired Immunodeficiency syndrome, AIDS) là một bệnh dịch tòan cầu gây nên do một loại virus mới được phát hiện gần đây có tên là virus thiếu hụt miễn dịch người týp I (Human Immunodeficiency Virus 1, HIV-1). Đây là một virus thuộc họ retrovirus tức những virus RNA có mang một enzym độc đáo là enzym sao chép ngược (reverse transcriptase) có khả năng tổng hợp DNA chuỗi kép đặc trưng cho virus từ genom RNA của mình. DNA mới này sẽ gắn vào genom của tế bào chủ và trở thành khuôn để sản xuất nguyên liệu RNA cho virus con. Virus con hình thành sẽ tạo chồi ở màng tế bào chủ và tế bào chủ cũng sẽ cung cấp vật liệu để thành lập vỏ virus.
Retrovirus được chia làm 3 nhóm: (1) oncovirus, bao gồm tất cả các virus sinh ung thư như virus bệnh bạch cầu tế bào T người (Human T cell Leukemia Virus I, HTLV-I); (2) spumavirus, là những virus mà hiện nay chưa thấy gây bệnh gì, và (3) lentivirus, trong đó có HIV-1.
Lentivirus gây những “nhiễm trùng chậm” tức là virus tồn tại một thời gian khá lâu trong cơ thể mới tạo ra các biểu hiện lâm sàng. HIV-1 là lentivirus gây bệnh ở người được khám phá đầu tiên và cũng là loại đầu tiên tác động lên các lympho bào.
Khỉ và các loại linh trưởng (primates) nuôi trong chuồng là những động vật rất dễ bị mắc bệnh thiếu hụt miễn dịch và người ta đã phân lập được một lentivirus giống HIV từ khỉ maccacus có thể gây hội chứng giống AIDS trên khỉ (người ta gọi là AIDS khỉ). Tại châu Phi, các nhà nghiên cứu cũng đã tìm thấy một virus có họ hàng rất gần với virus AIDS khỉ nói trên và gọi là SIV-1agm; SIV-1agm hình như không gây bệnh trên con vật sống trong thiên nhiên nhưng có khả năng gây bệnh khi ta tiêm vào khỉ macacus.
Năm 1985, người ta đã tìm thấy kháng thể chống HIV trong huyết thanh những cô gái điếm sống ở vùng Tây Phi, huyết thanh này cho phản ứng vớI SIV-1agm mạnh hơn với HIV. Kết quả là một lentivirus mới được phát hiện và được đặt tên là HIV-2, vì virus này cũng gây hội chứng giống AIDS cho người.
Dịch tễ học AIDS
Trước tiên, một điều thực sự khủng khiếp hiện nay là virus gây bệnh AIDS, tức HIV, đang lan tràn khắp thế giới với tốc độ khá nhanh mà sự ngăn chặn không phải là một việc làm đơn giản. Theo một tài liệu dịch tễ học công bố trên tờ Scientific American năm 1988 tại Hoa Kỳ, Jonathan M. Mann, James Chin, Peter Piot và Thomas Quinn cho biết rằng đến năm 1988 có hơn 250.00 trường hợp mắc bệnh được thống kê trên khắp thế giới, bên cạnh đó, có khoảng từ 5 đến 10 triệu người nhiễm HIV. Năm năm sau tình trạng đã trở nên xấu hơn nhiều. Liên minh chính sách AIDS tòan cầu (Global AIDS Policy Coalition) đã ước tính rằng vào cuối năm 1987 số người nhiễm HIV khoảng 7 triệu, nhưng đến cuối năm 1992 thì đã lên đến khoảng 110.5 triệu, tức tăng khoảng gấp 3 lần. Mặc dù có một số thuốc chống virus cũng như một số phương tiện khác có thể giúp phần nào đời sống, hầu hết người nhiễm đã đi đến tình trạng bi quan là tử vong. Cho đến năm 1993 có khoảng 3 triệu người mắc bệnh ở giai đoạn toàn phát, trong đó đa số đã chết. Các tính toán đã thông báo rằng vào năm 2001 số người nhiễm HIV là hơn 40 triệu.
Sự lan truyền của HIV-1
HIV-1 có thể phân lập từ tinh dịch, chất tiết cổ tử cung, tế bào lympho, huyết tương, dịch não tủy, nước mắt, nước bọt, nước tiểu và sữa mẹ. Nhưng không phải tất cả các dịch này đều có thể truyền bệnh bởi vì nồng độ virus trong chúng rất khác nhau, vì thế chỉ có tinh dịch, máu và có thể cả dịch cổ tử cung đã được chứng minh là có thể truyền bệnh.
Cách truyền phổ biến nhất của virus trên thế giới (Bảng 10.4) là quan hệ tình dục dù đồng giới hay khác giới. Việc lây truyền cũng có thể xảy ra qua đường dùng chung kim tiêm giữa những người tiêm chích do nghiện ngập hoặc những bệnh nhân được điều trị ở bệnh viện không thực hiện đúng qui trình vô trùng. Việc truyền bệnh từ mẹ sang con trong quá trình mang thai hoặc lúc sinh đẻ là đường lây chủ yếu đối với AIDS trẻ em. Ngoài ra chúng ta còn nghe nói đến những trường hợp bị lây bệnh do nhận máu, sản phẩm máu, nhận cơ quan ghép hoặc tinh dịch có HIV.
|
Tỉ lệ % bệnh nhân |
Hoa kỳ |
Anh |
|
Nam tình dục đồng giới/lưỡng giới Người nghiện tiêm chích tĩnh mạch Bệnh nhân mắc bệnh ưa cháy máu Người nhận máu có HIV Người tình dục khác giới Các loại khác Nam Nữ |
66 17 1 2 4 3 93 7 |
87,5 1.5 4 2 3.5 0.5 96.5 3.5 |
Bảng. Đặc diểm của bệnh nhân AIDS ở người lớn
Ngoài ra, người ta đã ghi nhận có một số ca nhân viên y tế có phản ứng huyết thanh dương tính do kim đâm hoặc dính máu bệnh nhân. Tuy nhiên, đường truyền theo muỗi, rệp, truyền qua hồ bơi, qua dùng chung dụng cụ ăn uống, dụng cụ vệ sinh hoặc thở chung không khí với bệnh nhân thì chưa được chứng minh.
Hình ảnh lâm sàng của nhiễm HIV-1
AIDS không phải là hậu quả độc nhất của nhiễm HIV-1: virus có thể gây ra nhiều bệnh cảnh mà nhìn chung thì tiên lượng đều xấu.
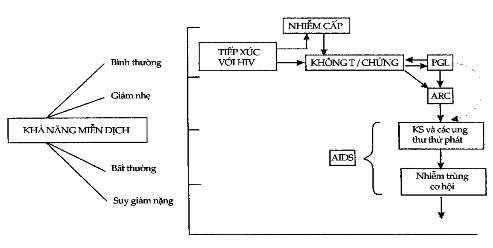
Hình. Các giai đoạn lâm sàng của nhiễm HIV-1; PGL = Bệnh lý hạch toàn thân kéo dài; ARC = Phức hợp cận AIDS; KS = U Kaposi.
Bệnh cảnh sốt có nổi hạch cấp tính có thể xảy ra thoáng qua trên 10-20% bệnh nhân trong những tuần lễ đầu tiên sau khi nhiễm HIV-1. Xét nghiệm máu ngoại biên cho thấy có 50% tế bào lymphô không điển hình, đồng thời có gia tăng số lượng tế bào T ức chế vào thời điểm này. Hầu hết những người huyết thanh dương tính rồi sẽ không có triệu chứng gì, ít nhất là trong một thời gian ngắn, và sau đó sự xuất hiện của AIDS có lẽ sẽ phụ thuộc vào các yếu tố kèm theo như cơ địa di truyền, bị kích thích lặp đi, lặp lại của kháng nguyên ngoại lai hoặc mang thai.
Sau một thời gian tiềm tàng kéo dài khoảng từ vài tháng đến 7 năm hay hơn nữa, những người nhiễm HIV-1 sẽ đi vào một quá trình bệnh lý gọi là bệnh lý hạch toàn thân kéo dài (persistent generalized lymphadenopathy, PGL). Các nghiên cứu trên những bệnh nhân đồng tính luyến ái nam bị PGL cho thấy rằng có khoảng 10-25% những người này sẽ tiến triển qua AIDS trong vòng 3 năm.
Một số người huyết thanh dương tính có thể có các biểu hiện khác như sưng hạch, ỉa chảy, ra mồ hôi đêm, nhiễm candida miệng và sụt cân mà không giải thích được nguyên nhân. Người ta gọi phức hợp cận AIDS đối với những trường hợp có ít nhất hai triệu chứng lâm sàng và hai hoặc nhiều hơn các dấu hiệu cận lâm sàng liệt kê ở.
HIV cũng là một virus hướng thần kinh; do đó người ta đã thông báo gặp những bệnh cảnh thần kinh như viêm màng não vô trùng cấp, bệnh lý não, bệnh lý tủy sống và bệnh thần kinh ngoại biên trên người bị nhiễm HIV vào giai đoạn sớm. Ngoài ra, vào giai đoạn muộn còn có thể thấy viêm màng não mạn tính, bệnh lý não mạn tính và trì trệ tinh thần.
Các biểu hiện lâm sàng chính của AIDS là ung thư và nhiễm trùng cơ hội. Hiện nay, chẩn đoán AIDS được thiết lập đối với những người có: (1) bệnh lý thể hiện rõ nét thiếu hụt miễn dịch tế bào ở mức độ vừa và nặng như viêm phổi do pneumocystis carinii hoặc u Kaposi; và (2) không tìm thấy các nguyên nhân khác của sự thiếu hụt miễn dịch tế bào cũng như nguyên nhân của giảm sức đề kháng đối với nhiễm trùng.
|
Hai triệu chứng lâm sàng |
+ Hai bất thường về xét nghiệm |
|
Sốt và/hoặc ra mồ hôi đêm (>3 tháng) Mệt người Sút cân (>10% trọng lượng cơ thể) Sưng hạch (>3 tháng) Ỉa chảy không rõ nguyên nhân |
Giảm lymphô bào Giảm tiểu cầu Giảm tế bào T giúp đỡ Tăng gammaglobulin máu Giảm khả năng chuyển dạng lymphô bào Dị ứng da với các kháng nguyên gặp lại |
Bảng. Chẩn đoán phức hợp cận AIDS
Chẩn đoán bị loại bỏ nếu tất cả các xét nghiệm cận lâm sàng nói lên tình trạng thiếu hụt miễn dịch đều âm tính.
U kaposi là loại u thường được đề cập nhất, nhưng các loại u khác cũng càng ngày càng được mô tả nhiều hơn như: u lymphô non-Hodgkin, u tế bào vảy ở miệng và trực tràng hậu môn.
Nhiễm trùng cơ hội trong AIDS có thể xảy ra ở bất cứ cơ quan nào nhưng cơ quan thường bị nhất là phổi, ống tiêu hóa và hệ thần kinh trung ương. Ngoài nhiễm trùng cơ hội, các cơ quan này còn có thể bị thâm nhiễm bởi u hoặc bị tác động trực tiếp của HIV-1 mà hệ thần kinh trung ương là một ví dụ điển hình.
Trẻ bị AIDS do mẹ truyền sang thường phát bệnh vào tuổi trung bình khoảng 6 tháng, trong khi đó trẻ sơ sinh nhiễm bệnh do truyền máu thì phát bệnh sau khoảng 12-15 tháng. Cả hai nhóm đều có bệnh cảnh lâm sàng giống nhau: trẻ không phát triển và hầu như tất cả đều có nhiễm candida ở miệng cũng như nhiễm trùng sinh mủ lặp đi lặp lại. Viêm phổi kẽ mãn tính là bệnh cảnh rất đặc trưng. Vào giai đoạn muộn, nhiễm trùng cơ hội điển hình có thể xuất hiện những u Kaposi và các ung thư khác thì hiếm khi gặp ở các trẻ này.
Tiên lượng đối với AIDS thật buồn thảm: nói chung là sẽ chết, và thời gian sống sót tùy thuộc vào biểu hiện lâm sàng. Thời gian sống còn đối với người bị nhiễm phổi do pneumocystis carinii là 9-12 tháng, đối với các nhiễm trùng cơ hội khác là 6-12 tháng và đối với u Kaposi là 20-30 tháng.
Miễn dịch học của AIDS
HIV-1 chui vào các tế bào thích hợp nhờ gắn glycoprotein của mình vào một receptor trên bề mặt tế bào, đó là phân tử CD4. Những tế bào có mang kháng nguyên CD4 đều có khả năng nhiễm HIV-1: điển hình là tế bào lymphô T giúp đỡ, một số tế bào B, đại thực bào, tế bào thần kinh đệm, và ngoài ra một số tế bào biểu mô của đại - trực tràng cũng mang CD4 với mật độ thấp.
Những bệnh phối hợp HIV (HIV-associated diseases) được đặc trưng bởi những tổn thương của chức năng miễn dịch (Bảng 10.6). Những tổn thương này xảy ra do sự suy giảm số lượng tế bào CD4+, nhất là tế bào T giúp đỡ. Khi tế bào T giúp đỡ bình thường được kích thích bởi kháng nguyên chúng đáp ứng bằng cách phân bào và giải phóng các lymphokin, bao gồm interleukin-2, interferon và yếu tố phát triển tế bào B (B cell growth factor, BCGF): những chất này điều hòa sự phát triển, trưởng thành và hoạt hóa các tế bào lympho khác, các tế bào mono cà đại thực bào.
Tế bào T gây độc sau khi được hoạt hóa sẽ tiêu diệt các tế bào bị nhiễm virus, trong khi đó đại thực bào hoạt hóa tiêu hủy các vi khuẩn nội bào như Mycobacterium tuberculosis. Còn interferon, một lymphokin khác thì kích thích sự tiêu hóa của tế bào giết tự nhiên (NK cell) và đồng thời tham gia kiểm soát sự hình thành ung thư.
Như vậy, tác động nổi bật nhất của HIV là nhằm đến đáp ứng qua trung gian tế bào T. Các thử nghiệm in vitro có thể cho thấy đáp ứng tăng sinh đối với kháng nguyên lặp lại bị biến đổi do giảm sản xuất IL-2 ngay cả trên bệnh nhân nhiễm HIV-1 chưa có triệu chứng. Trong quá trình diễn tiến bệnh, bên cạnh sự xuất hiện các triệu chứng mới là sự suy giảm số lượng tuyệt đối của tế bào CD4+, nhất là tế bào T giúp đỡ. Bởi vì trong các nhiễm trùng virus khác có thể có tăng số lượng tế bào CD8+ (chủ yếu là tế bào ức chế và gây độc) trong vòng hai tuần sau khi nhiễm, nhưng ở đây khi bệnh nhân chưa có triệu chứng thì số lượng tế bào lymphô và các tiểu quần thể của chúng vẫn còn bình thường.
|
Giảm số lượng tuyệt đối tế bào lymphô CD4+ Giảm đáp ứng tăng sinh đối với kháng nguyên hòa tan Thay đổi phản ứng quá mẫn muộn ở da Giảm sản xuất interferon khi đáp ứng với kháng nguyên Hoạt hóa tế bào B đa clôn cùng với tăng sản xuất Ig ngẫu nhiên Giảm đáp ứng dịch thể khi gây miễn dịch Các bất thường khác Giảm lymphô bào Giảm đáp ứng tăng sinh in vitro đối với mitogen tế bào T và kháng nguyên cùng loài Giảm đáp ứng tăng sinh đối với mitogen tế bào B đặc hiệu Giảm sản xuất interleukin-2 Giảm tính gây độc tế bào với tế bào nhiễm virus Tăng lượng phức hợp miễn dịch Giảm hoạt tính tế bào NK Giảm hóa hướng động monocyte |
Bảng. Các bất thường miễn dịch chủ yếu trong AIDS.
Khi bệnh nhân tiến triển đến giai đoạn phức hợp cận AIDS thì các xét nghiệm về chức năng tế bào T in vitro như đáp ứng với mitogen và sản xuất lymphokin bị giảm sút và bệnh nhân mất phản ứng với các thử nghiệm da quá mẫn muộn. Các chức năng của tế bào mono/đại thực bào ngày càng trở nên bất thường và hoạt tính của tế bào NK cũng bị giảm sút. Sinh thiết hạch bạch huyết cho thấy hình ảnh những nang lớn trong đó có thâm nhiễm tế bào lymphô CD8+, giảm tế bào CD4+ và phá hủy cấu trúc lưới bình thường.
Giải thích đơn giản nhất về nguyên nhân của những thay đổi này là tình trạng thiếu hụt miễn dịch gây ra do tác dụng phá hủy của HIV trên tế bào T giúp đỡ, tế bào mono và đại thực bào. Tình trạng giảm sản xuất lymphokin và giảm hoạt hóa đại thực bào là do nhiễm trùng virus, nấm và vi khuẩn nội bào tồn tại lâu dài. Bệnh nhân đôi khi có biểu hiện giảm tế bào trung tính hoặc giảm tiểu cầu; mà bệnh sinh có thể liên quan đến phức hợp miễn dịch.
Sau khi nhiễm HIV một thời gian ngắn, đáp ứng tạo kháng thể vẫn chưa thay đổi, do đó mà kháng thể chống protein vỏ và lõi virus là bằng chứng chính để chẩn đoán nhiễm virus. Về sau, sự hoạt hóa đa clôn đối với tế bào B được phản ánh qua sự gia tăng nồng độ Ig ở 80-90% bệnh nhân AIDS. Nguyên nhân của điều này chưa được hiểu rõ nhưng có lẽ là liên quan trực tiếp đến sự hoạt hóa tế bào B của HIV-1, và có thể trong phối hợp với virus Epstein-Barr. Tuy nhiên, đáp ứng đối với những kháng nguyên mới bị giảm sút, và ngay cả trong những bệnh nhân bị nhiễm trùng cơ hội lan rộng có thể không có tí kháng thể nào xuất hiện làm cho việc chuẩn đoán huyết thanh học kinh điển không thể tin cậy được trên bệnh nhân AIDS.
Phát hiện nhiễm HIV
Kháng thể chống HIV thường xuất hiện khoảng 3 tuần đến 3 tháng sau khi bị nhiễm và sau đó thì tồn tại mãi hầu như suốt đời. Đây là kháng thể chống các glycoprotein vỏ điển hình (gp120 và gp41). Mặc dù kháng thể trung hòa có thể định lượng được nhưng nồng độ thấp và không có ý nghĩa gì trong thời điểm hiện nay. Cũng như trong các nhiễm trùng virus khác, kháng thể chống HIV là bằng chứng trực tiếp của nhiễm trùng đã mắc. Tuy nhiên, không có kháng thể không có nghĩa là không có sự hiện diện của virus.Trên một số bệnh nhân người ta thấy vắng mặt các kháng thể đặc hiệu. Trong số này kể cả những người chỉ mới nhiễm virus được có vài tuần nên sự sản xuất kháng thể chưa đủ để có thể phát hiện được; và những người ở giai đoạn cuối của AIDS, lúc đó mức kháng thể giảm sút nhiều hoặc biến mất.
Kháng nguyên virus, nhất là kháng nguyên lõi của HIV-1 (gp41) cũng có mặt trong huyết thanh nhưng chỉ phát hiện được vào giai đoạn có thừa kháng thể đối với p24, điều này xảy ra vào lúc ban đầu của nhiễm trùng và trước khi bệnh tiến triển sang phức hợp cận AIDS hoặc AIDS.
Các hướng điều trị AIDS
Những kiến thức về đường xâm nhập của HIV vào tế bào CD4+ và cách thức nhân lên của chúng đã giúp chúng ta tìm ra các biện pháp điều trị có hứa hẹn.
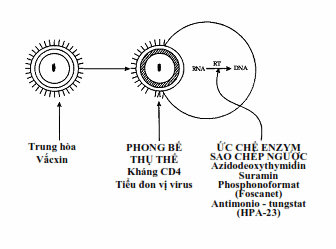
Hình. Các phương pháp điều trị nhằm ngăn ngừa hoặc loại trừ nhiễm HIV-1. (RT = enzym sao chép ngược).
Sự gắn của virus vào phân tử CD4 trên bề mặt tế bào có thể ức chế được nhờ kháng thể chống vỏ virus hay chống receptor. Trong việc phòng bệnh, kháng thể chống virus phải là kháng thể trung hòa, và mục tiêu của vắc-xin thích hợp là tạo ra một kháng thể như vậy.
Các vacxin cổ điển dùng virus chết hoặc giảm độc lực hình như không có giá trị trong trường hợp AIDS. Tính chất mong manh của vỏ HIV làm cho nó có tính sinh miễn dịch kém. Đồng thời khả năng biến đổi kháng nguyên của retrovirus rất nguy hiểm trong trường hợp của HIV, nhất là khi cũng đột biến để trở lại dạng hoạt động. Do đó, vacxin HIV không được có những đoạn RNA có khả năng nhân lên. Việc dùng kỹ thuật DNA tái tổ hợp đã tạo ra được nhiều sản phẩm có thể dùng để sản xuất vắc xin, nhưng tất cả đều trong giai đoạn thí nghiệm.
Ức chế nhân lên của virus có thể thực hiện được bằng cách ức chế hoạt tính của enzym sao chép ngược (reverse transcriptase) là enzym retrovirus duy nhất không có ở thú vật. Có nhiều thuốc ức chế được enzym sao chép ngược trong phòng thí nghiệm nhưng trong cơ thể thì tác dụng rất kém hoặc không tác dụng. Azidothymidin (AZT) là thuốc đang thông dụng trên thị trường có tác dụng ức chế sự nhân lên của virus. Nó là chất đồng dạng của thymidin lấy được từ DNA tiền virus. Tuy nhiên, AZT không thể chữa khỏi AIDS vì nó không diệt tận gốc được genom của virus. Ngoài ra, tác dụng độc của nó đối với tủy xương đã làm hạn chế việc dùng thuốc lâu dài nhất là ở những cá thể chưa có triệu chứng.
Một biện pháp khác quan trọng không kém sự phòng ngừa nhân lên của virus là xây dựng lại hệ thống miễn dịch của cơ thể chủ. Người ta đã thử dùng IL-2, interferon hoặc ghép tủy nhưng chưa thấy thành công nào rõ rệt. Trong điều trị nên phối hợp việc xây dựng lại hệ thống miễn dịch với liệu pháp chống virus.
Nhiễm trùng trên cơ thể suy giảm miễn dịch
Những người bị suy giảm miễn dịch tự nhiên hoặc do dùng thuốc thường rất dễ nhiễm trùng. Những bệnh nhân này có thể bị nguy cơ từ hai nguồn: các tác nhân nhiễm trùng thường gặp (thường gây bệnh cho cả người lành và bệnh nhân) và các nhiễm trùng “cơ hội” (tức là các vi sinh vật thường không có khả năng gây bệnh nhưng khi cơ thể bị suy yếu về mặt miễn dịch thì chúng nhân cơ hội đó dễ gây bệnh).
Chúng ta phải luôn lưu ý đến những nhiễm trùng cơ hội do thuốc gây ra. Theo một khảo sát trên 75 bệnh nhân bị mắc các bệnh “miễn dịch” (như bệnh chống màng đáy cầu thận, lupus ban đỏ hệ thống…) được điều trị bằng các thuốc ức chế miễn dịch thì tỉ lệ nhiễm trùng là 3,7 lần/người; hoặc 0,74 lần/người/tuần có suy giảm miễn dịch. Vào khoảng 2/3 số biến chứng nhiễm trùng gây ra bởi các vi khuẩn “thông thường” tức là các mầm bệnh đối với người bình thường. Các tác nhân cơ hội chiếm 1/3, trong đó có một số nhiễm trùng cơ hội rất nặng (chiếm 11% toàn bộ các nhiễm trùng biến chứng). Trong số 10 bệnh nhân chết do nhiễm trùng trong nhóm bệnh nhân này, có đến 8 người chết do nhiễm trùng cơ hội: một điều đáng lưu ý là ½ số vi sinh vật gây chết người chỉ tìm thấy khi mổ tử thi.
Nhiều nghiên cứu đã tổng kết để đưa ra các mô hình nhiễm trùng có thể dùng trong chẩn đoán đối với các cơ thể chủ lực bị ức chế miễn dịch.
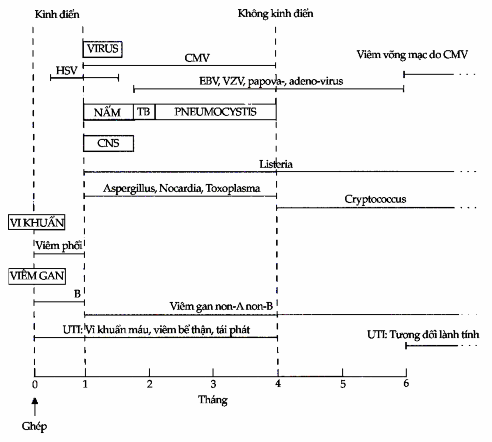
Hình. “Lịch” xuất hiện của nhiễm trùng trên bệnh nhân ghép thận
HSV = Virus Herpes Zoster; CMV = Virus Cytomegalovirus; EBV = Virus Epstein-Barr; VZV = Virus Varicella Zoster; UTI = Nhiễm trùng đường tiểu.
Những bệnh nhân được nghiên cứu kỹ nhất là bệnh nhân ghép thận. Vào tháng đầu sau khi ức chế miễn dịch, các nhiễm trùng cơ hội hầu như không có. Thay vào đó nguyên nhân nhiễm trùng chính là nhiễm trùng do vết thương phẩu thuật, do các ống xông hoặc nhiễm trùng phổi sau phẩu thuật. Giữa tháng thứ nhất và tháng thứ tư sau khi ức chế miễn dịch, nhiễm trùng cytomegalovirus chiếm ưu thế trong bối cảnh có thể có nhiều nhiễm trùng khác như nhiễm nấm, virus và đơn bào: đây là giai đoạn nhiễm trùng nguy hiểm nhất. Nhiễm trùng từ tháng thứ tư trở đi có thể xếp thành 3 nhóm: nhóm 1 là nhiễm virus mạn tính, đặc biệt là CMV; nhóm 2 là nhiễm trùng cơ hội thỉnh thoảng, mà đáng chú ý nhất là nhiễm Pneumocystis carinii. Cryptococcus neoformans và Listeria monocytogenes; và nhóm 3 là các nhiễm trùng thường gặp trong cộng đồng.
Trong cơ thể có hai cổng vào chính đối với các vi sinh vật cơ hội: vùng mũi họng hầu và phần dưới ống tiêu hóa. Hít các vi khuẩn đang sống trong vùng mũi họng hầu vào phổi là cơ chế thường gặp dẫn đến viêm phổi, còn sự lan tỏa vi khuẩn từ đường tiêu hóa thì thường gây nhiễm trùng huyết. Phổi là nơi nhiễm trùng phổ biến nhất. Hình ảnh lâm sàng không đặc hiệu: sốt, khó thở và ho khan trên một bệnh nhân có thâm nhiễm phổi lan tỏa trên phim X-quang. Cấy đờm và cấy máu thường không giúp tìm ra vi sinh vật gây bệnh. Cần phải dùng những phương pháp phức tạp hơn như rửa phế quản – phế nang hay sinh thiết phế quản mới mong chẩn đóan được nguyên nhân. Sau khi đã loại trừ các vi khuẩn gây bệnh thường gặp nhất là CMV, aspergillus, candida hoặc pneumocystis carinii. Chúng ta cần nhận rõ tầm quan trọng của chẩn đóan và điều trị sớm (nếu được) khi thấy rằng những nhiễm trùng phổi như vậy thường mang lại hậu quả rất xấu cho bệnh nhân suy giảm miễn dịch: tỉ lệ tử vong chung là 50-65%.
Bài viết cùng chuyên mục
Kỹ thuật DNA tái tổ hợp và miễn dịch lâm sàng
Kỹ thuật DNA tái tổ hợp, dựa vào việc sử dụng plasmid như các phương tiện để truyền các đoạn DNA lạ, ví dụ gen người.
Sản xuất kháng huyết thanh cho các phòng thí nghiệm miễn dịch lâm sàng
Hỗn dịch tế bào lách của con vật được gây mẫn cảm, có chứa nhiều tế bào B chịu trách nhiệm sản xuất nhiều kháng thể, chống nhiều epitope khác nhau.
Định typ HLA miễn dịch
Hiện nay, việc định týp HLA được thực hiện bằng kỹ thuật PCR, để phát hiện gen HLA, kỹ thuật này tốn kém hơn nhưng có độ chính xác và độ nhạy cao hơn.
Đánh giá tế bào trung tính và tế bào mono
Thực bào là chức năng ăn vật lạ của một tế bào nào đó, khả năng ăn này có thể xác định được bằng cách ủ tế bào thực bào, với các hạt trơ như hạt latex, hoặc vi khuẩn.
Khảo sát lymphô bào miễn dịch
Có hai loại phản ứng da in vivo, được dùng để phát hiện lympho bào T mẫn cảm đặc hiệu, đó là: thử nghiệm nội bì, dùng kháng nguyên tiêm vào lớp nội bì.
Khảo sát phức hợp miễn dịch
Hiện nay, trên thế giới, ta đã có bán những sản phẩm chuẩn, cho những phòng thí nghiệm miễn dịch đặc biệt chuyên khoa.
Khảo sát bổ thể miễn dịch
Định lượng C3 và C4, bằng phương pháp hóa miễn dịch, là các xét nghiệm có ích nhất, trên thế giới hiện nay đã sẵn có các huyết thanh chứng quốc tế.
Phát hiện tự kháng thể
Yếu tố thấp một kháng thể IgM, phản ứng với Ig,G đóng vai trò kháng nguyên sẽ cho phản ứng với IgG, ngưng kết mạnh hơn là với IgG người còn nguyên bản.
Kháng thể đối với kháng nguyên ngoại sinh
Thử nghiệm kích thích provocation test, tức thử nghiệm kích thích niêm mạc mũi hoặc niêm mạc phế quản bằng kháng nguyên, là một thử nghiệm khá phổ biến.
Khảo sát định tính immunoglobulin
Trong trường hợp không có bất thường chuỗi nặng, kháng huyết thanh chuỗi nhẹ tự do, tức không phản ứng với chuỗi nhẹ cố định vào chuỗi nặng.
Định lượng immunoglobulin và các protein đặc hiệu khác
Kỹ thuật thường được dùng phổ biến nhất, là miễn dịch kết tủa, tủa miễn dịch được hình thành khi kháng nguyên, và kháng thể, kết tủa tương ứng.
Đại cương các kỹ thuật miễn dịch
Một số xét nghiệm sẽ trở nên vô ích, nếu chúng ta yêu cầu không đúng lúc, đúng chỗ, các phân chia sẽ giúp lâm sàng có được chỉ định thích hợp.
Một số hiệu quả thuận lợi của phản ứng tự miễn
Tìm được những chất tải, hiệu quả nhất cũng như các tá chất thích hợp, để có thể gây phản ứng ở mức độ mong muốn.
Điều trị bệnh miễn dịch
Phản ứng tự miễn cũng có thể xảy ra nếu tế bào T hoặc B tự phản ứng mang một idiotyp phổ biến có phản ứng chéo với idiotyp trên kháng thể hoặc với cấu trúc trên vi khuẩn.
Chẩn đoán và tiên lượng bệnh miễn dịch
Tự kháng thể cón có giá trị tiên lượng, trường hợp một đứa trẻ, có anh chị em mắc bệnh đái đường phụ thuộc insulin, nó có chung HLA với anh chị.
Cơ chế bệnh sinh bệnh miễn dịch
Tế bào B tự phản ứng, tế bào T hiệu quả và tự kháng nguyên bình thường, vẫn có mặt trong cơ thể, nhưng không được khởi động.
Bệnh nguyên bệnh miễn dịch
Có những mô hình bệnh tự miễn ngẫu nhiên, trên động vật, rất có ích cho chúng ta nghiên cứu, đầu tiên là bệnh tuyến giáp tự miễn trên gà trống Obese.
Tính di truyền của bệnh tự miễn
Hoạt động của yếu tố di tryền, là xu hướng phối hợp của bệnh tự miễn, đối với các tính đặc hiệu HLA, Haplotyp B8, DR3 xuất hiện với tần suất cao.
Sự sắp xếp các bệnh tự miễn thường gặp ở người
Những cơ quan đích thường gặp, trong bệnh đặc hiệu cơ quan, là tuyến giáp, tuyến thượng thận, dạ dày và tuyến tụy.
Bằng chứng về tính chất gây bệnh của phản ứng tự miễn
Khi có được dòng động vật cảm thụ thích hợp rồi, ta còn có thể gây bệnh thụ động bằng cách truyền tế bào T mẫn cảm cho con vật khác.
Tính tự miễn dịch
Sự hình thành một đáp ứng kháng thể bình thường, đối với đa số kháng nguyên protein đòi hỏi sự tham gia của 3 loại tế bào B, T, và tế bào trình diện kháng nguyên.
Thiếu hụt miễn dịch tiên phát
Đối với những trường hợp thiếu hụt kháng thể bẩm sinh, nhiễm trùng tái đi tái lại bắt đầu xuất hiện, trong khoảng thời gian từ tháng thứ 4 đến 2 tuổi.
Đại cương thiếu hụt miễn dịch
Một đứa trẻ, hay một người lớn, sẽ bị nghi ngờ là thiếu hụt miễn dịch, khi trên cơ thể xuất hiện những nhiễm trùng lặp đi lặp lại, tồn tại kéo dài, trầm trọng hoặc bất thường.
Các phản ứng quá mẫn không đặc hiệu
Một cơ chế không đặc hiệu khác đã tham gia gây quá mẫn, đó là trường hợp thiếu các protein bất hoạt C3b, làm cho phản ứng hoạt hóa bổ thể không dừng lại.
Quá mẫn miễn dịch typ V (Quá mẫn kích thích)
Trên thực nghiệm, người ta đã phát hiện được thêm một số kháng thể kích thích hoạt động chức năng của tế bào, qua các kháng nguyên có trên bề mặt tế bào.
Quá mẫn miễn dịch typ IV (Quá mẫn muộn)
Cần luôn nhớ rằng, tổn thương quá mẫn, là hậu quả của phản ứng quá mức, giữa kháng nguyên, với cơ chế miễn dịch tế bào vẫn còn bình thường
Quá mẫn miễn dịch typ III
Kháng thể và kháng nguyên tạo thành phức hợp, phức hợp này hoạt hóa bổ thể đồng thời tác động gây giải phóng các amin hoạt mạch, làm tăng tính thấm thành mạch.
Quá mẫn miễn dịch typ II
Phản ứng truyền máu đối với các thành phần khác của máu, như bạch cầu, tiểu cầu cũng có thể xảy ra, nhưng hậu quả của nó không nặng nề như phản ứng đối với hồng cầu.
Quá mẫn miễn dịch typ I
Một khi IgE gắn thụ thể Fcε trên tế bào mast, và tế bào ái kiềm, sự mất hạt sẽ xảy ra khi có liên kết chéo, giữa các phân tử IgE.
Đại cương về quá mẫn miễn dịch
Qúa mẫn là một đặc điểm của cá thể, và nó xảy ra khi có tiếp xúc với kháng nguyên lần thứ hai.
Miễn dịch chống nấm
Nhiễm nấm có thể gây nhiều hậu quả, thường chỉ đáp ứng miễn dịch đặc hiệu chống nấm cùng với thuốc chống nấm tại chỗ, có thể tiêu diệt được bệnh nhiễm nấm cạn.
Miễn dịch chống ký sinh trùng
Bệnh nhân chống chọi với nhiễm ký sinh trùng đơn bào, bằng những phản ứng tương tự như trong nhiễm vi khuẩn, có một số đơn bào có cơ chế tồn tại độc đáo.
Miễn dịch chống vi khuẩn
Một số vi khuẩn xâm nhập qua đường niêm mạc, có thể tạo ra các protease để ly giải kháng thể IgA tiết, neisseria gonorrhea, neisseria meningitis.
Miễn dịch chống virus
Virus Epsptein-Barr dùng thụ thể của C3b tức CR2, còn HIV thì lại dùng thụ thể CD4 để làm nơi xâm nhập vaof tế bào đích, trong hệ thống miễn dịch.
Đại cương miễn dịch chống vi sinh vật
Đối với nhiễm trùng, một cân bằng được duy trì giữa sức chống đỡ của cơ thể, và khả năng của vi sinh vật cố gắng để vượt qua sức chống đỡ đó.
Cytokin kích thích tạo máu
Các cytokin khác nhau kích thích, sự phát triển, và trưởng thành của nhiều dòng tế bào máu khác nhau.
Các cytokin trung gian và điều hòa miễn dịch thu được
Mặc dù lúc đầu người ta phát hiện ra IL 2, như là một yếu tố phát triển tế bào T, nhưng thật ra IL 2 có nhiều chức năng trong đáp ứng miễn dịch thu được.
Các cytokin trung gian và điều hòa miễn dịch bẩm sinh
Có 2 loại thụ thể của TNF, loại có trọng lượng phân tử 55 kD có tên là THF RI, và loại có trọng lượng phân tử 75 kD có tên là TNF RII.
Đại cương về Cytokin
Các cytokin này do các tế bào đệm, bạch cầu, và một vài tế bào khác của tủy xương sản xuất, chúng có thể kích thích sự phát triển, và biệt hóa của bạch cầu non.
Sự hình thành phức hợp tấn công màng C5 9
Sau khi C5b gắn màng, C6 và C7 đến gắn vào C5b để tạo C5b67, C5b67 tác động với C8 để tạo C5b678, đơn vị này tạo phản ứng trùng hợp phân tử C9.
Con đường hoạt hóa bổ thể không cổ điển (alternative pathway)
Không nhất thiết phải có phản ứng kháng nguyên, kháng thể, nên phản ứng có thể xảy ra tức thì, và cơ thể được bảo vệ theo cơ chế không đặc hiệu.
Con đường hoạt hóa bổ thể cổ điển (classical pathway)
Một phân tử IgM pentamer, kết hợp với kháng nguyên, là có thể cố định bổ thể, nhưng đối với IgG, thì phải có phân tử IgG được gắn với kháng nguyên ở vị trí gần nhau.
Đại cương bổ thể
Các protein của hệ thống bổ thể tạo thành hai chuỗi enzym, mà người ta gọi là con đường cổ điển, và con đường không cổ điển, để tạo nên hai cách phân cách hai phân tử C3
Tế bào trình diện kháng nguyên
Tế bào hình sao được tìm thấy dưới lớp biểu bì, và trong đa số các cơ quan, ở đó chúng được đặt ở tư thế sẵn sàng để bắt giữ kháng nguyên.
Tế bào lymphô hệ miễn dịch
Tế bào lymphô bao gồm nhiều tiểu quần thể khác nhau, khác biệt về chức năng, về sản phẩm protein nhưng không phân biệt được về hình thái.
Đại cương các tế bào chủ yếu của hệ thống miễn dịch
Tế bào tham gia vào đáp ứng miễn dịch thu được, bao gồm các lymphô bào đặc hiệu kháng nguyên, tế bào trình diện kháng nguyên.
Một số kháng nguyên quan trọng
Người ta biết nhiều về cấu trúc của vùng H 2I của chuột, hơn vùng tương đương, với vùng này ở người là vùng HLA D.
Các tính chất của kháng nguyên
Một kháng nguyên protein phức tạp, có thể nhiều quyết định kháng nguyên khác nhau, do đó mà nó có thể kích thích tạo ra nhiều loại kháng thể khác nhau.
Sự kết hợp kháng nguyên kháng thể
Khả năng trung hòa độc tố, và vi sinh vật của kháng thể, luôn phụ thuộc vào sự gắn kết chặt chẽ của chúng vào kháng thể.
Cấu trúc phân tử của kháng thể
Các glycoprotein huyết tương, hoặc huyết thanh trước đây thường được phân chia theo tính chất hòa tan, của chúng thành albumin và globulin.
Phân bố tự nhiên và sản xuất kháng thể
Một người lớn khoẻ mạnh nặng 70 kg sản xuất khoảng 3g kháng thể mỗi ngày, khoảng 2 phần 3 là kháng thể có tên là IgA, được sản xuất bởi tế bào B.
Các con đường và cơ chế tái tuần hoàn và homing của tế bào lympho
Tế bào T nguyên vẹn có xu hướng homing, và tái tuần hoàn qua các cơ quan lymphô ngoại biên, để ở đó chúng sẽ nhận dạng, và đáp ứng với kháng nguyên.
Các cơ quan mô lymphô của hệ thống miễn dịch
Cơ quan và mô lymphô ngoại biên, bao gồm hạch bạch huyết, lách, hệ thống miễn dịch da, và hệ thống miễn dịch niêm mạc.
Các giai đoạn của đáp ứng miễn dịch thu được
Những nguyên lý cơ bản của thuyết chọn clôn, đã dần được chứng minh một cách thuyết phục, qua nhiều thí nghiệm, và tạo nên nền tảng cho quan niệm hiện nay.
Các thành phần tế bào của hệ thống miễn dịch thu được
Có một nhóm tế bào lymphô thứ ba, là tế bào giết, đây là những tế bào tham gia vào hệ thống miễn dịch bẩm sinh, chống lại nhiễm trùng virus.
Các đặc điểm chính của đáp ứng miễn dịch thu được
Tất cả đáp ứng miễn dịch bình thường, sẽ phai nhạt dần theo thời gian, để trả lại hệ miễn dịch ở trạng thái nghỉ ban đầu, tình trạng này gọi là hằng định nội môi.
Các kiểu đáp ứng miễn dịch thu được
Sự nhấn mạnh về kháng thể, trong lý thuyết này, đã dẫn đến sự thừa nhận chung, tầm quan trọng của miễn dịch dịch thể.
Tính miễn dịch bẩm sinh và thu được
Các cơ chế của miễn dịch tự nhiên, cung cấp sức đề kháng ban đầu đối với nhiễm trùng, đáp ứng miễn dịch thu được đến muộn hơn, với sự hoạt hoá tế bào lymphô.
Đại cương miễn dịch
Chức năng sinh lý của hệ thống miễn dịch, là bảo vệ một cơ thể chống lại các vi sinh vật gây bệnh, xâm nhập vào cơ thể đó.